KRAS G12C突变非小细胞肺癌靶向治疗进展与展望
KRAS G12C突变是非小细胞肺癌中重要的驱动基因变异之一,在亚洲NSCLC患者中约占4%。由于其独特的分子结构特征,KRAS G12C长期以来被视为“不可成药”靶点,给临床治疗带来诸多挑战。
- 最新进展
一、引言
KRAS G12C突变是非小细胞肺癌(NSCLC)中重要的驱动基因变异之一,在亚洲NSCLC患者中约占4%。由于其独特的分子结构特征,KRAS G12C长期以来被视为“不可成药”靶点,给临床治疗带来诸多挑战。近年来,随着靶向药物研发的突破,KRAS G12C抑制剂相继问世,显著改善了该类患者的预后。随着医保政策的覆盖,药物可及性进一步提升,推动KRAS G12C突变肺癌的诊疗格局发生深刻变革。本文系统梳理KRAS G12C突变晚期NSCLC的核心诊疗痛点、靶向药物的临床应用进展、医保政策带来的影响、一线联合治疗的探索前景,以及未来面临的挑战与突破方向,以期为临床精准诊疗提供参考。
二、KRAS G12C突变晚期NSCLC的临床挑战
KRAS G12C靶点因其独特的结构特征,长期面临药物研发困境。KRAS蛋白表面光滑且存在动态构象变化,缺乏明显的结合位点;同时KRAS与内源性配体GDP/GTP亲和力极强,小分子药物难以竞争结合,进一步增加了研发难度。在KRAS G12C靶向药物问世前,此类患者多参照驱动基因阴性人群的治疗策略,以化疗和免疫治疗为主,但整体疗效欠佳。化疗方案的客观缓解率(ORR)普遍低于20%,中位无进展生存期(PFS)仅为4~6个月;免疫联合化疗的获益亦有限,难以满足临床需求。
此外,KRAS G12C突变晚期NSCLC患者中肝转移、脑转移及STK11/KEAP1共突变发生率较高,这类人群治疗难度大且缺乏针对性干预措施。肝转移病灶血供丰富、微环境复杂,常规治疗难以有效控制;脑转移患者受血脑屏障限制,多数药物穿透性不足;STK11/KEAP1共突变患者肿瘤异质性强、预后差,化疗联合免疫治疗的有效性进一步降低。尽管KRAS G12C抑制剂的问世显著改善了患者预后,但相较于EGFR、ALK等其他驱动基因阳性肺癌的靶向治疗,KRAS G12C抑制剂单药的疗效仍存在明显差距,需探索更多联合策略以提升治疗效果。
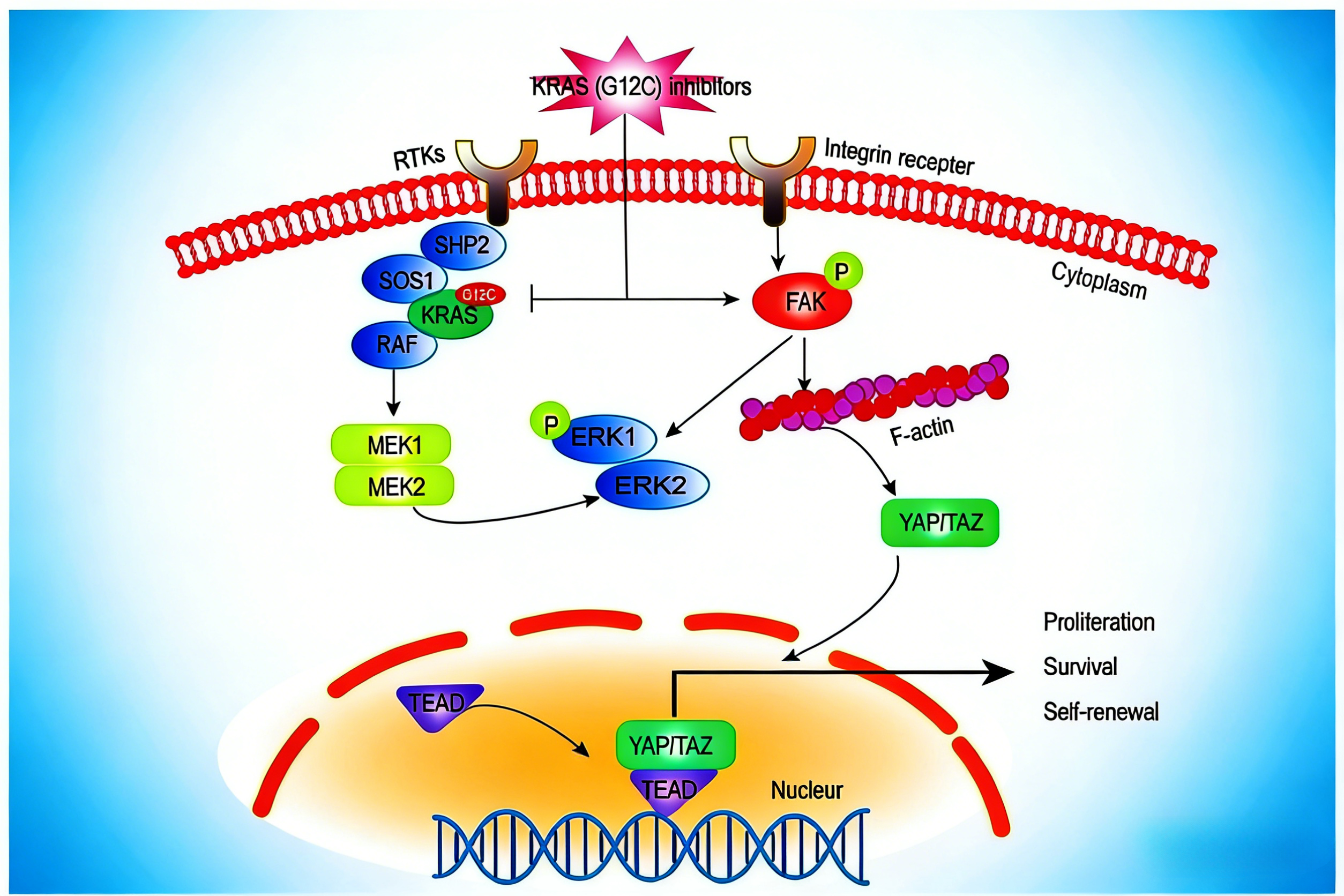
三、KRAS G12C抑制剂的分子机制与临床优势
新型KRAS G12C抑制剂(如索托拉西布、阿达格拉西布)通过选择性靶向KRAS G12C突变蛋白的SWITCH II口袋,将蛋白稳定锁定于GDP结合的失活状态,阻断其向GTP结合的活性构象转化,进而抑制下游信号通路的异常激活。其分子结构设计中的双甲基取代哌嗪结构,不仅增强了与突变蛋白的结合亲和力,还形成低能量稳定构象,延长药物作用时间并提升结合稳定性。
临床研究数据显示,在既往经治的KRAS G12C突变晚期NSCLC患者中,该抑制剂治疗的ORR达52%,中位PFS提升至9个月以上,中位总生存期(OS)达14.1个月。对于肝转移和脑转移患者,ORR分别达65.2%和61.1%,填补了这类难治性人群的精准治疗空白。在安全性方面,该药物对野生型KRAS蛋白结合力低,减少了正常细胞损伤,血液学毒性较低,不良反应多控制在1-2级,未观察到因不良反应导致永久停药的案例。
值得注意的是,该抑制剂的II期注册研究前瞻性纳入化疗、免疫治疗失败的患者,其中近20%为既往接受过三线及以上治疗的人群,基线特征更贴合真实世界中多线治疗的困境。即使在此背景下,药物仍实现52%的ORR及14.1个月的中位OS。此外,各亚组均能获得一致性疗效获益,STK11共突变亚组ORR达43.8%,KEAP1共突变亚组ORR为40%,打破了同类药物在共突变人群中治疗受限的瓶颈。
四、KRAS G12C & CRBN Binding 试剂盒在耐药机制研究中的应用
随着KRAS G12C抑制剂临床应用的拓展,耐药问题逐渐显现。获得性耐药机制包括继发性KRAS突变(如G12D、G12V、G13D等)、旁路信号激活(如MET扩增、EGFR激活)及组织学转化等。在针对耐药机制的研究中,准确评估KRAS G12C蛋白与E3泛素连接酶的相互作用对于理解降解途径介导的耐药逆转具有重要意义。
人KRAS G12C & CRBN Binding 试剂盒(GTP load)为这一研究提供了标准化检测工具。该试剂盒基于KRAS G12C蛋白在GTP结合状态下的构象特征,模拟靶向降解剂或内源性降解途径中靶蛋白被招募至CRBN连接酶的过程。通过时间分辨荧光共振能量转移(TR-FRET)技术,可定量检测KRAS G12C与CRBN的结合活性,用于评估候选化合物是否通过泛素-蛋白酶体途径诱导KRAS降解。在耐药机制研究中,该试剂盒可用于验证耐药后出现的KRAS二次突变是否影响与E3连接酶的相互作用,或用于筛选能够克服耐药的新型降解分子。
五、结语
KRAS G12C突变曾长期面临“不可成药”困境,近年来随着靶向药物的研发突破,已逐步实现从后线向前线的治疗前移。医保政策的全面覆盖显著提升了药物可及性,使更多患者获益。未来需进一步开展基于生物标志物的分层研究,完善全程化管理模式,探索联合治疗策略(如联合SHP2抑制剂、PD-1抑制剂、化疗等)以克服耐药,最终实现KRAS G12C突变肺癌患者的精准治疗与长期生存获益。













