HICA均相化学发光技术原理与应用进展
化学发光免疫分析是将高灵敏度的化学发光检测与高特异性的免疫反应相结合的分析技术,广泛应用于抗原、抗体、小分子及药物的定量检测。
- 最新进展
一、引言
化学发光免疫分析(CLIA)是将高灵敏度的化学发光检测与高特异性的免疫反应相结合的分析技术,广泛应用于抗原、抗体、小分子及药物的定量检测。根据是否存在分离清洗步骤,化学发光可分为异相法和均相法两大类。目前临床检验主流平台多采用异相化学发光技术,但其依赖物理分离和洗涤步骤,存在仪器复杂、检测耗时、操作繁琐等局限。均相化学发光技术无需分离清洗,在液相中直接完成检测,为简化操作流程、实现快速检测提供了新途径。本文系统阐述均相化学发光的技术原理、分类特点及临床应用进展。
二、化学发光技术的分类
化学发光免疫分析可按照不同标准进行分类。根据分离清洗步骤,分为异相化学发光法和均相化学发光法。异相法依赖于抗原抗体复合物与游离成分的物理分离,通常将反应物固定于固相载体,通过磁分离、过滤或洗涤去除未结合成分,因此检测步骤多、仪器结构复杂、耗时长。均相法无需分离清洗,在液相中直接检测,具有操作简便、检测快速、仪器便携等优势。
根据发光体系的不同,化学发光可分为间接化学发光、直接化学发光、电化学发光和光激化学发光。间接化学发光采用酶标记抗体,通过酶催化底物产生发光;直接化学发光采用吖啶酯等标记物,在氧化剂作用下直接发光;电化学发光通过电极反应触发发光;光激化学发光则需外界光源激发产生单线态氧介导的能量传递。
三、均相化学发光的技术原理
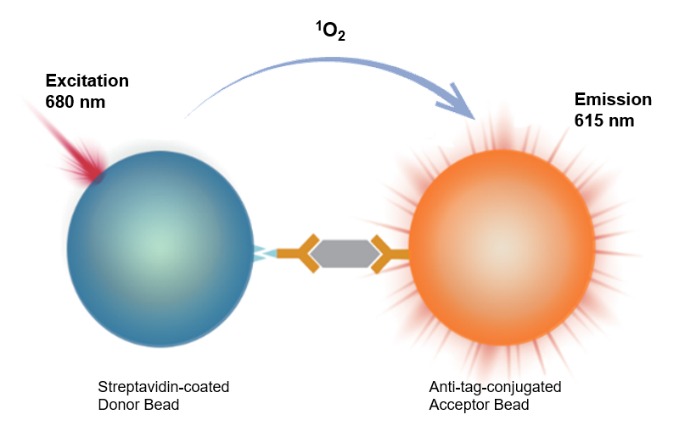
均相化学发光技术的核心在于实现液相中免疫反应与信号产生的耦合,无需物理分离步骤。其中最具代表性的是基于氧通道的发光氧通道免疫分析(LOCI)技术。该技术采用两种功能化微球:敏感珠包被有链霉亲和素并含光敏染料,化学珠包被检测抗体并含发光染料。检测时,样本中的待测抗原与生物素化抗体及化学珠结合形成夹心复合物,随后加入敏感珠,通过生物素-链霉亲和素结合形成免疫复合物聚集体。在680nm激发光照射下,敏感珠内的光敏染料产生单线态氧,单线态氧扩散至化学珠,触发发光染料产生612nm化学发光信号。发光强度与抗原浓度呈正比。
该技术的核心创新在于利用单线态氧的短寿命扩散特性实现能量传递,只有在两种微球近距离聚集时才能产生可检测信号,从而在液相中实现了特异性检测。这一机制完全避免了分离洗涤步骤,实现了真正的均相检测。
四、均相化学发光的技术优势
与异相化学发光相比,均相技术具有显著优势。首先,无需分离洗涤步骤,简化了操作流程,缩短了检测时间,单个样本检测可在15-30分钟内完成。其次,仪器结构简化,无需复杂的液路系统和磁分离模块,降低了设备成本和故障率,更适用于床旁快速检测(POCT)场景。第三,液相反应环境更接近生理状态,避免了固相包被可能引入的构象改变,有利于保持抗原抗体结合活性。第四,反应体系封闭,减少了操作过程中的污染风险,提高了检测结果的可靠性。
五、均相化学发光的临床应用
均相化学发光技术在临床检验领域具有广阔应用前景。在传染病筛查方面,可用于乙肝、丙肝、艾滋病等标志物的快速检测;在肿瘤标志物检测中,可用于甲胎蛋白(AFP)、癌胚抗原(CEA)等的定量分析;在心肌标志物检测领域,适用于肌钙蛋白、肌红蛋白等的床旁快速检测;在治疗药物监测(TDM)中,可用于免疫抑制剂、抗生素等血药浓度监测。
该技术尤其适用于基层医疗和急诊场景,其操作简便、检测快速的特点可显著提升服务效率。随着技术进步,检测灵敏度和线性范围不断提升,已能满足主流临床项目的检测需求。
六、均相化学发光的技术挑战
尽管均相化学发光技术优势明显,但仍面临若干挑战。单线态氧的产生和传递对环境因素敏感,样本中的淬灭剂可能干扰信号检测。两种微球的稳定性及批间一致性对试剂盒质量控制提出更高要求。激发光源和检测光路的设计需要精密光学系统,增加了仪器开发的复杂性。此外,与传统异相平台相比,均相技术的项目覆盖度仍有待扩展。
七、展望
随着体外诊断(IVD)技术向快速化、便携化、智能化方向发展,均相化学发光技术迎来了重要发展机遇。未来技术突破将集中于新型发光探针的开发、信号放大策略的优化、多联检能力的拓展以及与微流控技术的融合。国产均相化学发光平台的成熟将为基层医疗和急诊救治提供更优解决方案,推动我国体外诊断产业向高质量方向发展。随着技术不断完善和临床应用深入,均相化学发光有望在POCT领域发挥更大作用。













