一、ACSS2概述
酰基辅酶A合成酶短链家族成员2(Acetyl-CoA Synthetase 2, ACSS2)是ACSS家族的重要成员,能够催化乙酸转化为乙酰辅酶A(acetyl-CoA)。作为哺乳动物中唯一已知能将游离乙酸转化为乙酰辅酶A的酶,ACSS2在能量代谢和表观遗传调控中扮演着双重角色。
ACSS2基因通过选择性转录起始位点产生两种亚型(1606 bp和2106 bp),主要在细胞核和细胞质中表达,在肝脏、肾脏和心脏中高表达,在脑和睾丸中中度表达。与主要定位于线粒体基质、参与乙酸氧化的ACSS1不同,ACSS2更侧重于脂质合成和蛋白乙酰化调控。

二、ACSS2的分子机制与代谢功能
2.1 乙酰辅酶A生成的关键节点
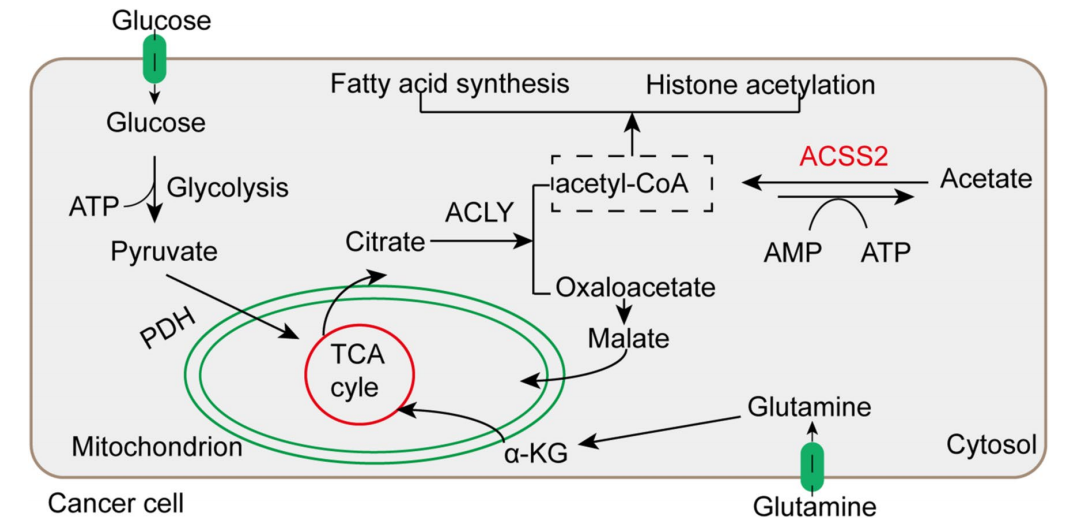
乙酰辅酶A是细胞代谢的核心中间产物,既是三羧酸循环(TCA循环)的底物,也是脂肪酸合成、胆固醇合成和组蛋白乙酰化的起始原料。在正常生理条件下,细胞主要通过葡萄糖分解产生丙酮酸,进而在线粒体中生成乙酰辅酶A。然而,在代谢应激条件下(如缺氧、营养缺乏),ACSS2介导的乙酸代谢途径成为维持细胞生存的重要替代机制。
ACSS2催化的反应具有可逆性:
2.2 双重功能:脂质合成与应激响应
ACSS2具有独特的双重功能特性:
在正常条件下,ACSS2主要作为细胞质内的脂质生成酶,促进脂质合成与储存。其表达受固醇调节元件结合蛋白(SREBPs)调控,当胆固醇或脂肪酸水平降低时,SREBPs被激活并转位至细胞核,促进ACSS2等脂质合成相关基因的表达。
在应激条件下(营养缺乏、缺氧、损伤),ACSS2转而作为调控因子,诱导脂肪酸氧化和自噬,维持能量稳态。这种功能转换使细胞能够根据营养状态和应激条件灵活调整代谢策略。
三、ACSS2与肿瘤代谢
3.1 肿瘤微环境中的代谢适应
肿瘤细胞常处于缺氧和营养缺乏的微环境中,ACSS2成为其维持生存和增殖的关键酶。研究表明,在缺氧条件下,肿瘤细胞对乙酸的依赖性显著增加,ACSS2表达上调,通过利用乙酸作为碳源进行脂肪酸合成。

胞依赖ACSS2利用乙酸合成脂肪酸(原图 media/image3.png)
ACSS2在多种肿瘤中高表达,包括乳腺癌、前列腺癌、胰腺癌等,其表达水平与肿瘤进展和预后相关。在代谢应激条件下,ACSS2敲除显著抑制肿瘤细胞生长,证明乙酸是肿瘤细胞重要的替代营养来源。
3.2 免疫调节功能
2023年发表在《Nature Cancer》的研究揭示了ACSS2在肿瘤免疫中的新功能。研究发现,抑制ACSS2不仅阻断肿瘤细胞的乙酸摄取,还能使肿瘤细胞从乙酸消费者转变为乙酸生产者,释放的乙酸可被肿瘤浸润淋巴细胞(TILs)利用,增强T细胞的效应功能和增殖能力。
这种"代谢免疫调节"模式为癌症治疗提供了新思路:靶向ACSS2既能抑制肿瘤代谢,又能增强抗肿瘤免疫反应,与化疗或免疫检查点抑制剂联用可能产生协同效应。
四、ACSS2与代谢性疾病
4.1 非酒精性脂肪性肝病(NAFLD)
ACSS2在肝脏脂质代谢中的重要作用使其成为NAFLD的潜在治疗靶点。高脂饮食条件下,肠道微生物将过量果糖代谢为乙酸等短链脂肪酸,经门静脉进入肝脏后,ACSS2将其转化为乙酰辅酶A,促进脂肪酸合成和脂肪肝形成。
ACSS2敲除小鼠在高脂饮食下表现出脂肪组织沉积减少,胆固醇和不饱和脂肪酸合成相关转录因子表达下降,提示抑制ACSS2可能改善NAFLD。
4.2 糖尿病与糖尿病肾病
ACSS2通过多种机制参与糖尿病及其并发症的发生发展:
- 胰岛素抵抗:ACSS2过表达促进脂质合成和脂肪沉积,释放促炎细胞因子,导致胰岛素抵抗
- 肾脏纤维化:脂质积累增加活性氧(ROS)和NLRP3炎症小体介导的肾脏纤维化
- mTOR通路激活:ACSS2介导的组蛋白乙酰化激活mTOR通路,抑制自噬,导致糖尿病肾病
五、ACSS2抑制剂的研究进展
| 药物/项目名称 | 开发阶段 | 适应症 |
|---|---|---|
| MTB-9655 | I期临床试验完成 → 推进至I/II期 | 晚期实体瘤(结直肠癌、乳腺癌、肺癌等) |
| 脑穿透性ACSS2小分子抑制剂(含AD-5584、AD-8007等) | 临床前研究完成(技术授权阶段) | 乳腺癌脑转移、脑部肿瘤 |
| Pep16(肽类抑制剂) | 计算机设计 / 体外验证 | 抗肿瘤 |
| CRD-1400 | 临床前研究 | 癌症 (如胶质母细胞瘤, 黑色素瘤, 乳腺癌等) |
| Asiatic acid | 临床前研究 | 糖尿病肾病(肾纤维化) |
| VY-3-135 | 临床前 / 工具化合物 | 肿瘤(代谢依赖性肿瘤) |
| ACSS2-IN-2 | 临床前 / 工具化合物 | 肿瘤(研究用途) |
| ACSS2抑制剂专利(WO20250186433) | 专利申请阶段 | 癌症、酒精中毒、CMV感染 |
六、总结与展望
ACSS2作为连接代谢与表观遗传的关键节点,在生理和病理条件下均发挥重要作用。其独特的双重功能——细胞质中的脂质合成与细胞核内的组蛋白乙酰化调控——使其成为代谢性疾病和肿瘤治疗的理想靶点。
当前研究趋势包括:
1. 精准医疗:基于ACSS2表达水平的患者分层,开发针对性治疗策略
2. 联合治疗:ACSS2抑制剂与化疗、免疫治疗或放疗的协同应用
3. 代谢-免疫偶联:深入探索ACSS2在肿瘤微环境中的免疫调节功能
4. 结构生物学:解析人源ACSS2晶体结构,指导下一代抑制剂设计
随着对ACSS2生物学功能认识的不断深入和特异性抑制剂的开发,针对这一靶点的治疗策略有望为代谢性疾病和癌症患者带来新的治疗选择。













