- 最新进展
- 产品信息
LIGHT蛋白(TNFSF14)的生物学特性与免疫调控功能研究
一、LIGHT蛋白的发现与基本特性
LIGHT(Lymphotoxin-like, exhibits inducible expression and competes with HSV glycoprotein D for HVEM)蛋白是肿瘤坏死因子超家族(TNFSF)的第14位成员,其研究始于20世纪末对TNF家族配体-受体系统的探索。1998年,研究者通过基因筛选首次发现这一具有独特免疫调节功能的分泌型蛋白,其命名体现了与单纯疱疹病毒糖蛋白D(gD)竞争结合HVEM受体的特性 。
从分子结构来看,LIGHT蛋白由240个氨基酸构成,呈现典型的II型膜蛋白特征:氨基端37个氨基酸构成胞内结构域,中间22个氨基酸形成跨膜区,羧基端181个氨基酸组成胞外功能域。值得注意的是,LIGHT可通过蛋白酶切割形成可溶性活性形式,这种双态表达模式使其能够同时参与局部细胞间信号传导和系统性免疫调节 。
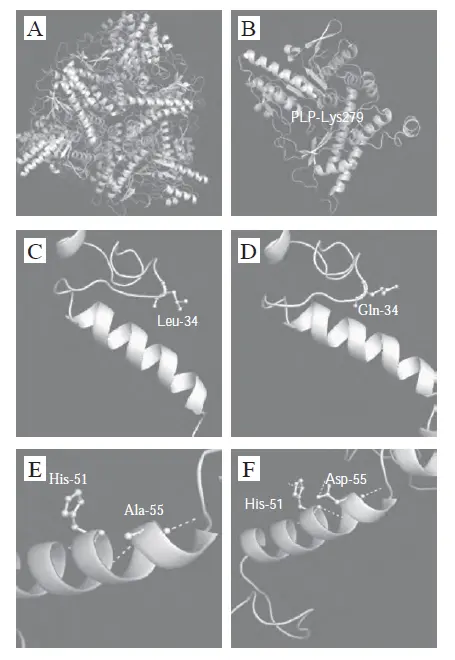
LIGHT蛋白三维结构示意图
二、分子作用网络与信号传导机制
2.1 受体系统
LIGHT蛋白通过双重受体系统发挥生物学效应:
- HVEM(单纯疱疹病毒进入介质):主要表达于T细胞、树突状细胞等免疫细胞表面
- LTβR(淋巴毒素β受体):广泛分布于基质细胞、上皮细胞及部分肿瘤细胞
这种双受体系统使LIGHT能够介导免疫细胞间的直接通讯(HVEM途径)以及免疫细胞与微环境的相互作用(LTβR途径)。特别值得注意的是,HVEM受体还参与调节BTLA(B and T lymphocyte attenuator)共抑制信号,形成复杂的免疫调节网络 。
2.2 信号转导通路
与受体结合后,LIGHT激活以下关键信号通路:
- NF-κB经典通路:通过TRAF2/5介导的IKK复合体激活,促进促炎因子表达
- 非经典NF-κB通路:经由NIK激酶激活p52/RelB二聚体,参与淋巴器官发育
- MAPK通路:调控细胞增殖与凋亡平衡
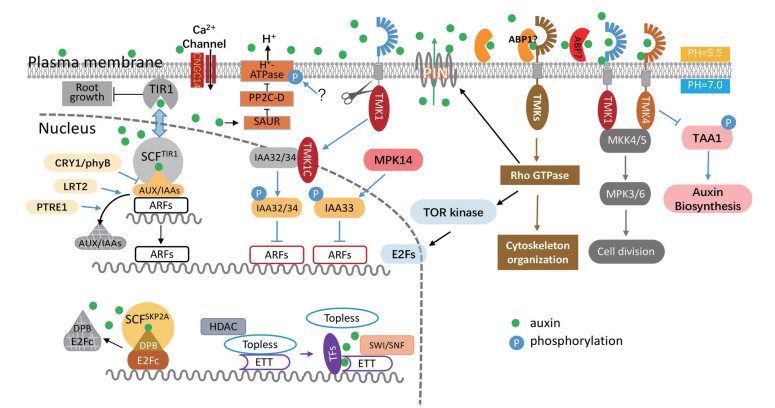
LIGHT信号通路示意图
三、免疫调节功能解析
3.1 适应性免疫调控
在T细胞免疫中,LIGHT通过HVEM提供共刺激信号,显著增强CD4+和CD8+ T细胞的活化与增殖。实验数据显示,LIGHT刺激可使T细胞IL-2分泌量提升3-5倍,同时促进记忆T细胞的形成。值得注意的是,这种激活作用具有剂量依赖性,过高浓度的LIGHT可能诱导活化诱导细胞死亡(AICD) 。
3.2 固有免疫参与
在自然杀伤(NK)细胞中,LIGHT通过LTβR途径刺激IFN-γ分泌,其效价可达基础水平的8-10倍。这种激活作用与NKG2D受体的协同效应,形成抗病毒和抗肿瘤的双重防御机制。此外,LIGHT还能增强树突状细胞的抗原呈递能力,促进CD80/CD86等共刺激分子的表达 。
3.3 炎症调节的双向性
LIGHT在炎症反应中表现出独特的双向调节特性:
- 促炎效应:通过LTβR诱导单核细胞分泌IL-6、TNF-α等炎症因子
- 抗炎作用:在慢性炎症中通过诱导调节性T细胞(Treg)扩增维持免疫稳态
这种特性使其在类风湿关节炎、炎症性肠病等自身免疫性疾病中呈现复杂的作用模式。
四、抗肿瘤作用机制
4.1 肿瘤微环境重塑
LIGHT可通过以下途径改变肿瘤免疫微环境:
- 促进三级淋巴结构(TLS)形成,提升肿瘤浸润淋巴细胞(TIL)密度
- 抑制MDSC(髓源抑制细胞)的免疫抑制作用
- 重塑肿瘤血管系统增强免疫细胞浸润
临床前研究显示,局部LIGHT过表达可使黑色素瘤模型小鼠的生存期延长40%-60% 。
4.2 直接抗肿瘤效应
通过LTβR信号,LIGHT可诱导多种实体瘤细胞(如结肠癌、肺癌)发生caspase依赖性凋亡。其机制涉及:
- 线粒体膜电位下降
- Bcl-2家族蛋白比例失衡
- ROS水平显著升高
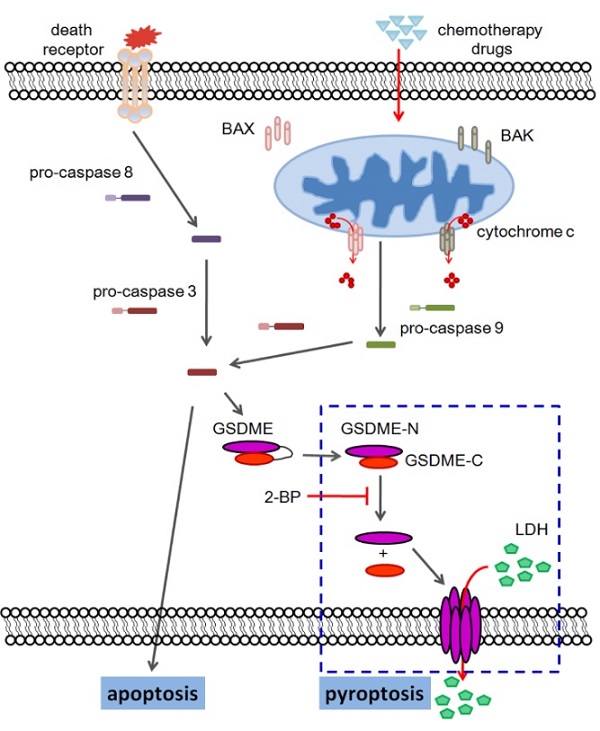
LIGHT诱导肿瘤细胞凋亡示意图
4.3 协同治疗潜力
在CAR-T治疗中,LIGHT共表达可显著增强效应细胞的肿瘤浸润能力和持久性。动物实验表明,这种改良型CAR-T的肿瘤清除效率提升2-3倍,且能有效克服免疫抑制微环境。
五、研究进展与转化前景
5.1 基础研究突破
近年研究揭示了LIGHT蛋白的若干新功能:
- 调控代谢重编程:影响T细胞的糖酵解通路
- 表观遗传调控:通过miRNA网络影响免疫记忆形成
- 微生物组互作:调节肠道菌群与免疫系统的动态平衡
5.2 临床转化方向
目前聚焦的转化研究方向包括:
- 重组LIGHT蛋白的局部给药系统开发
- 基于LIGHT信号通路的双特异性抗体设计
- 联合免疫检查点抑制剂(如PD-1抗体)的协同治疗方案
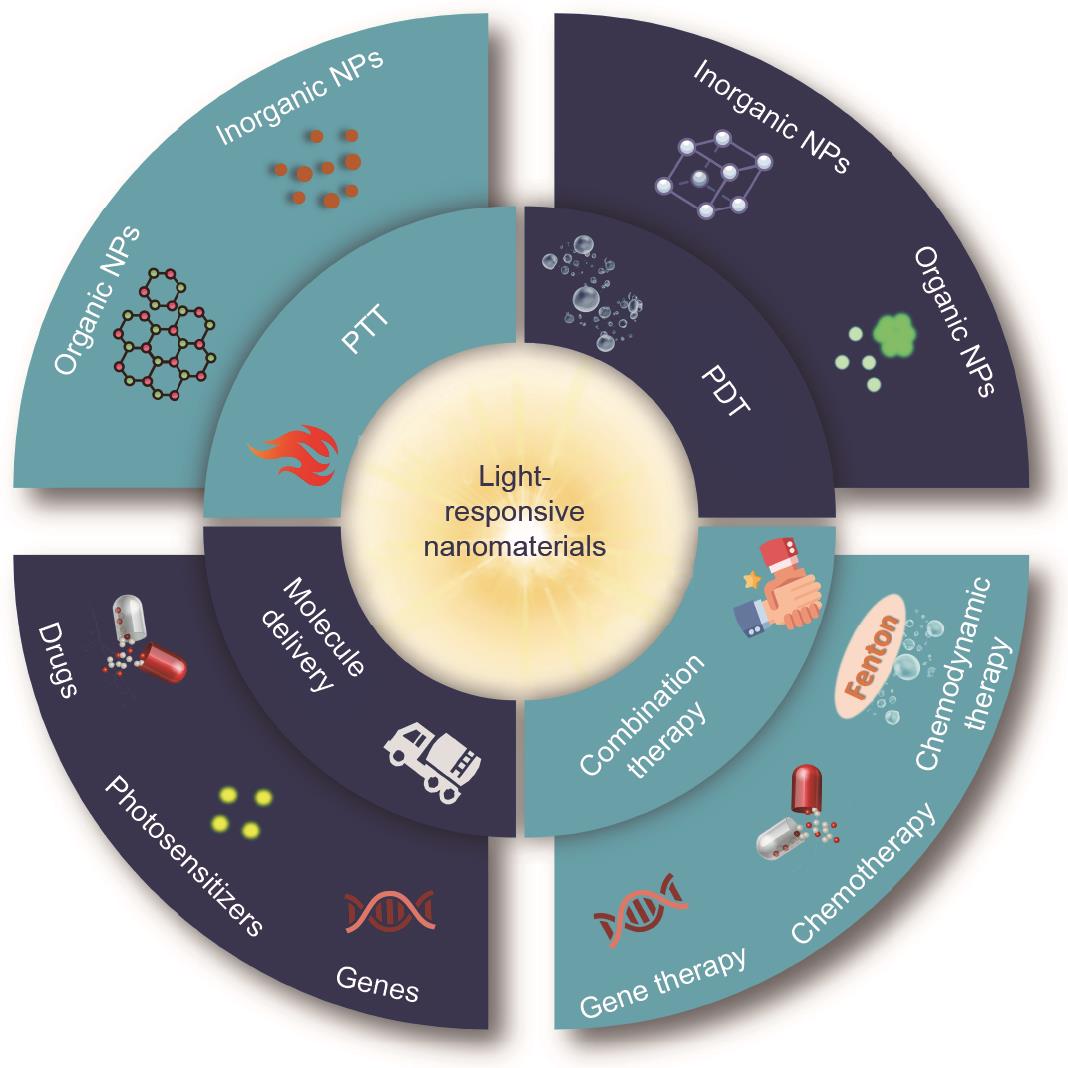
LIGHT蛋白临床应用策略图
六、挑战与展望
尽管LIGHT蛋白展现出广阔的临床应用前景,仍存在若干关键科学问题亟待解决:
- 系统毒性的控制:全身性LIGHT激活可能诱发细胞因子风暴
- 受体选择性的调控:HVEM与LTβR信号的平衡策略
- 生物标志物开发:预测治疗响应的分子标记物筛选
未来研究需要结合单细胞测序、类器官模型等新技术,深入解析LIGHT信号的时空动态特征。随着对LIGHT生物学特性的深入理解,这一分子有望成为新一代免疫治疗的核心靶点,为肿瘤和自身免疫性疾病的精准治疗提供新范式。













