EBV MHC-I四聚体技术突破:解码鼻咽癌免疫应答,赋能精准免疫治疗研发
Epstein-Barr病毒(EBV,人类疱疹病毒4型)作为首个被确认与人类肿瘤发生相关的DNA病毒,其致病机制与临床转化价值持续受到关注。流行病学数据显示,全球每年新增EBV相关恶性肿瘤病例约20万例,其所致死亡占恶性肿瘤相关死亡总数的1.8%。
- 最新进展
- 产品信息
EBV MHC四聚体
Epstein-Barr病毒(EBV,人类疱疹病毒4型)作为首个被确认与人类肿瘤发生相关的DNA病毒,其致病机制与临床转化价值持续受到关注。流行病学数据显示,全球每年新增EBV相关恶性肿瘤病例约20万例,其所致死亡占恶性肿瘤相关死亡总数的1.8%。EBV感染具有广泛组织嗜性,可诱发多类细胞来源的恶性肿瘤:包括B细胞淋巴瘤(如Burkitt淋巴瘤、经典霍奇金淋巴瘤)、NK/T细胞淋巴瘤(鼻型)、上皮细胞癌(鼻咽癌、胃腺癌)及间叶组织肿瘤(平滑肌肉瘤)等。值得注意的是,上皮细胞源性肿瘤占全部EBV相关恶性肿瘤的80%以上,其中鼻咽癌(NPC)组织中EBV DNA检出率高达90%以上,这使其成为EBV靶向免疫治疗领域的研究热点。
1.EBV生命周期与潜伏感染特征
EBV感染周期包含急性感染与潜伏感染两个阶段。病毒主要通过唾液传播,初始感染靶细胞为口咽部上皮细胞和B淋巴细胞,随后在B细胞中建立潜伏感染状态。在宿主免疫抑制或微环境改变等条件下,潜伏病毒可被激活进入裂解复制周期,通过表达病毒裂解期蛋白诱导宿主细胞恶性转化。这种动态的病毒-宿主相互作用构成了EBV相关肿瘤发生发展的分子基础。
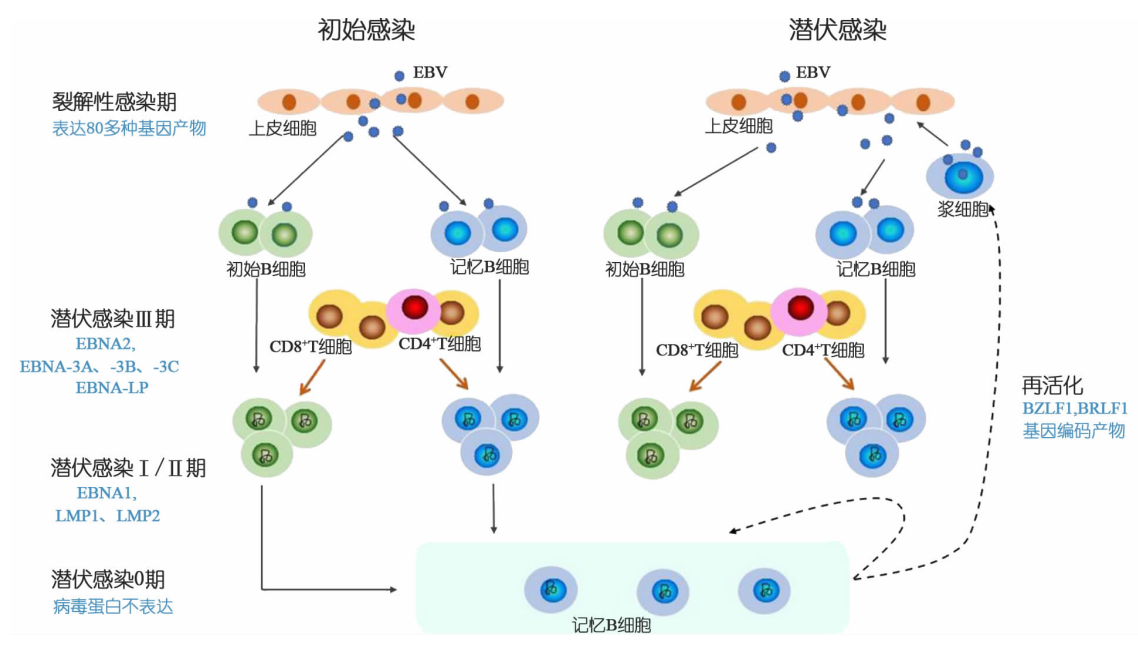
2. EBV免疫治疗关键靶点蛋白
EBV潜伏感染期可表达11种特征性病毒蛋白,包括6种核抗原(EBNA1、EBNA2、EBNA3A、EBNA3B、EBNA3C及EBNA-LP)、3种潜伏膜蛋白(LMP1、LMP2A、LMP2B)以及2种非编码RNA(EBER1、EBER2)。根据病毒蛋白表达谱差异,EBV潜伏感染可划分为三种生物学亚型:① 潜伏Ⅰ型仅表达EBNA1与EBERs,典型见于Burkitt淋巴瘤;② 潜伏Ⅱ型表达EBNA1、LMP1/2及EBERs,与鼻咽癌、霍奇金淋巴瘤等恶性肿瘤密切相关;③ 潜伏Ⅲ型呈现全基因表达模式(包括全部EBNAs、LMPs及EBERs),多见于免疫缺陷相关淋巴增殖性疾病。
值得关注的是,EBV基因组存在显著遗传异质性,其变异热点集中于LMP1、EBNA2/3家族等免疫调控相关基因,同时涉及BDLF3(编码包膜糖蛋白gp150)、BLLF1(编码gp350/200)、BNLF2a(免疫逃逸相关蛋白)及BZLF1/BRRF2等病毒复制关键基因。这些遗传变异直接影响病毒蛋白的免疫原性及致癌潜能,为精准免疫治疗靶点筛选带来挑战。
3. MHC-I四聚体技术推动鼻咽癌免疫治疗研发
CD8⁺ T细胞通过T细胞受体(TCR)特异性识别MHC-抗原肽复合物,触发对病毒感染细胞及肿瘤细胞的精准杀伤。基于该原理,Altman团队于1996年首次开发出MHC-抗原肽四聚体技术,通过流式细胞术实现单个细胞水平抗原特异性T细胞的直接检测与功能解析。相较于传统细胞因子分泌或细胞毒性检测,该技术可同步完成T细胞定量、表型分析及功能评估,已成为肿瘤免疫监测的核心工具。
研究团队针对中国人群高频HLA-A0201/A1101/A*2402等位基因,结合EBV致癌蛋白表位预测算法,构建了系列EBV特异性MHC-I四聚体试剂。该技术平台可高效解析EBV相关肿瘤(如鼻咽癌)中抗原特异性T细胞应答特征,为靶向EBV的疫苗开发、TCR-T细胞治疗及免疫疗效监测提供关键技术支撑。
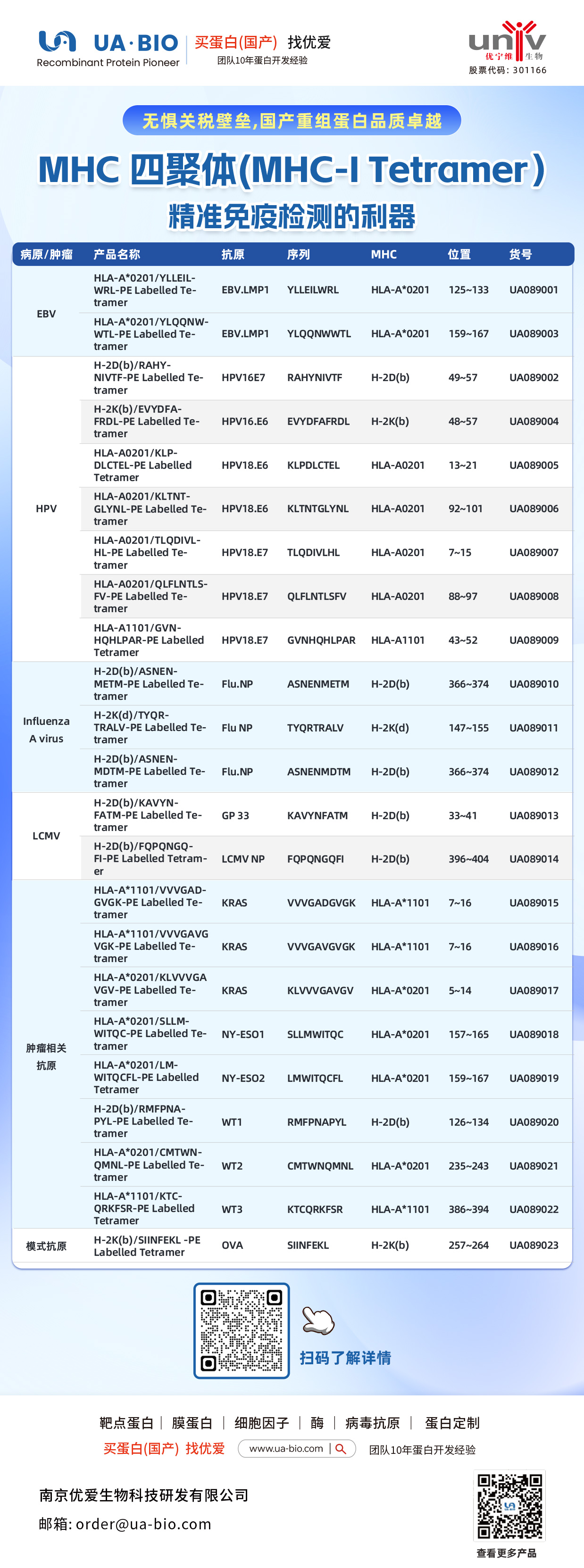
相关产品推荐
| 病原/肿瘤 | 产品名称 | 抗原 | 序列 | MHC | 位置 | 货号 |
| EBV | HLA-A*0201/YLELLVWRL-PE Labelled Tetramer | EBV.LMP1 | YLELLVWRL | HLA-A*0201 | 125-133 | UA089001 |
| EBV | HLA-A*0201/YLQQNWTL-PE Labelled Tetramer | EBV.LMP1 | YLQQNWTL | HLA-A*0201 | 159-167 | UA089003 |
| EBV | H-2Db(b)/RAHY-NIVTF-PE Labelled Tetramer | HPV16.E7 | RAHYNIVTF | H-2Db | 49-57 | UA089002 |
| HPV | H-2K(b)/EVYDFA-FRQL-PE Labelled Tetramer | HPV16.E6 | EVYDFARDL | H-2Kb | 48-57 | UA089004 |
| HPV | HLA-A*0201/KLP-DLCTL-PE Labelled Tetramer | HPV18.E6 | KLPDCTL | HLA-A*0201 | 13-21 | UA089005 |
| HPV | HLA-A*0201/KLTNT-GLYQL-PE Labelled Tetramer | HPV18.E6 | KLTNTGLYNL | HLA-A*0201 | 92-101 | UA089006 |
| HPV | HLA-A*0201/TLODIVIHL-PE Labelled Tetramer | HPV18.E7 | TLODIVIHL | HLA-A*0201 | 7~15 | UA089007 |
| HPV | HLA-A*0201/QFLNTL-FV-PE Labelled Tetramer | HPV18.E7 | QFLNTLFSV | HLA-A*0201 | 88-97 | UA089008 |
| HPV | HLA-A*1101/GVNHQLPAR-PE Labelled Tetramer | HPV18.E7 | GVNHQLPAR | HLA-A*1101 | 43-52 | UA089009 |
| Influenza A Virus | H-2D(b)/ASNENMETM-PE Labelled Tetramer | Flu.NP | ASNENMETM | H-2Db | 366-374 | UA089010 |
| Influenza A Virus | H-2K(d)/TYQR-TRALY-PE Labelled Tetramer | Flu.NP | TYQRTRALY | H-2Kd | 147-155 | UA089011 |
| Influenza A Virus | H-2D(b)/ASNEN-MDTM-PE Labelled Tetramer | Flu.NP | ASNENMDTM | H-2Db | 366-374 | UA089012 |
| LCMV | H-2D(b)/KAVYNFATM-PE Labelled Tetramer | GP 33 | KAVYNFATM | H-2Db | 33-41 | UA089013 |
| LCMV | H-2D(b)/FQPGQGFVK-PE Labelled Tetramer | LCMV NP | FQPGQGFVK | H-2Db | 396-404 | UA089014 |
| Tumor-related | HLA-A*1101/VVGADGVK-PE Labelled Tetramer | KRAS | VVGADGVK | HLA-A*1101 | 7~16 | UA089015 |
| Tumor-related | HLA-A*1101/VVGAGVGK-PE Labelled Tetramer | KRAS | VVGAGVGK | HLA-A*1101 | 7~16 | UA089016 |
| Tumor-related | HLA-A*0201/KLVVGAGV-PE Labelled Tetramer | KRAS | KLVVGAGV | HLA-A*0201 | 5~14 | UA089017 |
| Tumor-related | HLA-A*0201/SLLMWITQC-PE Labelled Tetramer | NY-ESO1 | SLLMWITQC | HLA-A*0201 | 157-165 | UA089018 |
| Melanoma | HLA-A*0201/LMWITQCFL-PE Labelled Tetramer | NY-ESO2 | LMWITQCFL | HLA-A*0201 | 159-167 | UA089019 |
| Melanoma | H-2Db(b)/MMFPNA-P1-PE Labelled Tetramer | WT1 | RMFPNAPL | H-2Db | 126-134 | UA089020 |
| Melanoma | HLA-A*0201/CMTWV-PE Labelled Tetramer | WT2 | CMTWVNMDM | HLA-A*0201 | 235-243 | UA089021 |
| Melanoma | HLA-A*1101/KTCQRKSF-PE Labelled Tetramer | WT3 | KTCQRKSF | HLA-A*1101 | 386-394 | UA089022 |
| Ovarian Cancer | H-2K(b)/SINFEKL-PE Labelled Tetramer | OVA | SINFEKL | H-2Kb | 257-264 | UA089023 |