- 最新进展
- 产品信息
最新进展
一、MSLN 的分子特征与研究价值
间皮素(Mesothelin,MSLN)是一种以糖基磷脂酰肌醇(GPI)锚定形式存在于细胞表面的糖蛋白,因其独特的表达模式而成为肿瘤治疗领域的研究热点。在正常生理状态下,MSLN 的组织表达范围极为有限,而在卵巢癌、乳腺癌、结直肠癌、胰腺癌等多种实体肿瘤中却呈现显著的过度表达特征,且其高表达水平与患者较低的存活率密切相关。这种肿瘤特异性的表达模式,使 MSLN 成为肿瘤靶向治疗的理想候选靶点,为开发精准抗癌策略提供了重要的分子基础。近年来的研究进一步发现,MSLN 在急性髓系白血病(AML)等血液系统恶性肿瘤中也存在异常高表达,这一发现突破了其仅作为实体瘤靶点的传统认知,拓展了其在肿瘤治疗中的应用前景。
二、MSLN 的结构解析与加工机制
(一)基因与蛋白的基本结构
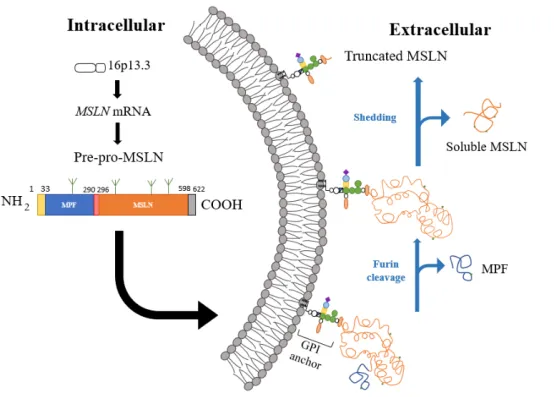
MSLN 基因定位于人类染色体 16p13.3 区域,其转录生成的 mRNA 经过翻译过程产生前体蛋白(Pre-pro-MSLN)。该前体蛋白的结构包含多个功能区域:N 末端的信号肽序列负责引导蛋白运输;中间区域包含巨核细胞增强因子(megakaryocyte-potentiating factor,MPF)结构域、呋喃蛋白酶(Furin)裂解位点以及成熟 MSLN 结构域;C 末端则带有 GPI 锚定序列,确保成熟蛋白能够锚定于细胞膜表面。在 Pre-pro-MSLN 的氨基酸序列中,存在四个潜在的糖基化位点,其中三个位于成熟 MSLN 结构域,这些糖基化修饰对 MSLN 的结构稳定性和功能发挥具有重要意义。
(二)蛋白加工与可溶性形式的产生
MSLN 的成熟过程经历了复杂的蛋白水解加工。当 Pre-pro-MSLN 被运输至细胞膜附近时,Furin 或其他特异性蛋白酶会识别并切割其呋喃裂解位点,将前体蛋白分解为可溶性的 MPF 和带有 GPI 锚定序列的成熟 MSLN。成熟 MSLN 通过 GPI 锚定与细胞膜结合,定位于细胞表面行使功能。此外,细胞膜表面的成熟 MSLN 还可被 ADAM17 转换酶进一步切割,从膜上脱落形成可溶性间皮蛋白相关肽(soluble mesothelin-related peptide,SMRP),这种可溶性形式可在体液中被检测到,为肿瘤的诊断和病情监测提供了潜在的生物标志物。
三、MSLN 的生物学功能与信号调控网络
(一)细胞黏附与肿瘤转移
MSLN 的重要生物学功能之一是通过与其他分子的相互作用介导细胞黏附。研究证实,MSLN 可与粘蛋白家族成员 CA125/MUC16 特异性结合,这种相互作用在体外实验中能够介导异型细胞间的黏附,被认为是卵巢癌等肿瘤发生腹膜转移的关键机制之一。动物实验也为 MSLN 的功能提供了有力证据:MSLN 基因敲除小鼠的腹膜腔内癌细胞生长受到显著抑制,而外源性补充 MSLN 蛋白或 MPF 则可促进肺癌细胞的生长和转移,表明 MSLN 在肿瘤微环境中通过增强细胞黏附和迁移能力,推动肿瘤的进展和扩散。
(二)信号通路的激活与肿瘤表型调控
MSLN 通过激活多条细胞内信号通路参与肿瘤细胞的生物学行为调控。细胞表面或可溶性 MSLN 可触发 Akt、ERK1/2 和 JNK 等信号通路的激活,这些通路通过下游分子的级联反应发挥多种生物学效应:一方面,通过上调 Bclxl/Bcl2 等抗凋亡蛋白的表达,同时抑制 Bim、Bad、Bax 等促凋亡基因的功能,减少肿瘤细胞的凋亡;另一方面,通过增加基质金属蛋白酶 7(MMP7)的表达,增强肿瘤细胞的迁移和侵袭能力。此外,MSLN 还可激活 p38、NF-κB 和 STAT3 等信号通路,NF-κB 的激活可促进 IL-6 等细胞因子的分泌,进一步维持细胞存活和增殖;STAT3 则通过促进 Cyclin E/CDK2 复合体的形成,加速细胞周期进程,推动肿瘤细胞的异常增殖。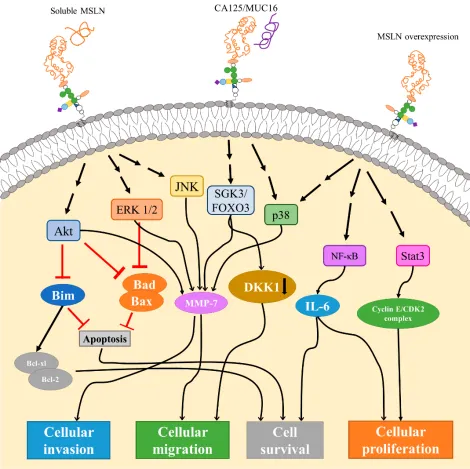

四、MSLN 靶向治疗的策略与研究进展
(一)抗体 - 药物偶联物(ADC)的开发
Anetumab ravtansine 是目前研究较为成熟的 MSLN 靶向 ADC 药物,其由靶向 MSLN 的单克隆抗体通过可切割连接子与微管蛋白抑制剂 dm4 偶联而成。该药物通过抗体与肿瘤细胞表面 MSLN 的特异性结合被内化进入细胞,释放出的 dm4 可与微管蛋白结合,破坏微管的正常组装,阻断细胞周期进程,最终诱导肿瘤细胞凋亡。这种 “精准递送” 的治疗模式在临床前研究中展现出良好的肿瘤杀伤效果和安全性,为实体瘤和血液肿瘤的治疗提供了新方向。
(二)细胞免疫治疗策略
嵌合抗原受体(CAR)修饰的免疫细胞疗法是 MSLN 靶向治疗的另一重要领域。研究者通过基因工程技术,将识别 MSLN 的单链抗体片段与免疫细胞激活信号域融合,构建出 CAR-T 细胞和 CAR-NK 细胞。这些修饰后的免疫细胞能够特异性识别并结合表达 MSLN 的肿瘤细胞,通过释放穿孔素、颗粒酶等细胞毒性分子直接杀伤肿瘤细胞。此外,双特异性 T 细胞结合分子(BITE)也被应用于 MSLN 靶向治疗,这类分子一端结合肿瘤细胞表面的 MSLN,另一端结合 T 细胞表面的 CD3 分子,从而将 T 细胞招募至肿瘤部位并激活其杀伤功能,在临床前研究中显示出显著的抗肿瘤活性。

五、总结与展望
MSLN 凭借其肿瘤特异性的表达模式和在肿瘤进展中的关键作用,已成为肿瘤免疫治疗领域的重要靶点。从结构解析到功能研究,从信号机制阐明到治疗策略开发,对 MSLN 的深入探索为理解肿瘤发生发展机制和开发新型靶向疗法提供了重要依据。尽管目前尚无 MSLN 靶向药物获批上市,但多种治疗策略在临床前研究和早期临床试验中展现出良好的应用前景。未来,随着对 MSLN 生物学功能的进一步揭示和治疗技术的不断优化,MSLN 靶向疗法有望在实体瘤和血液系统恶性肿瘤的精准治疗中发挥越来越重要的作用,为改善肿瘤患者的预后带来新的希望。
产品信息













