- 最新进展
- 产品信息
引言:为何卵巢癌免疫治疗需要更精准的T细胞检测工具?
卵巢癌作为妇科恶性肿瘤中最致命的一种类型,多数患者在确诊时已处于晚期,且易产生化疗耐药。近年来,免疫治疗为晚期卵巢癌患者带来了新的希望,尤其是基于T细胞的过继性免疫疗法和疫苗策略。然而,如何准确识别并扩增那些能够特异性识别卵巢癌相关抗原的T细胞,成为该领域的关键科学问题。MHC四聚体技术作为抗原特异性T细胞检测的“金标准”,正逐渐成为探索卵巢癌免疫应答机制和优化免疫治疗方案的重要工具。
何谓MHC四聚体技术?其工作原理如何支撑T细胞特异性识别?
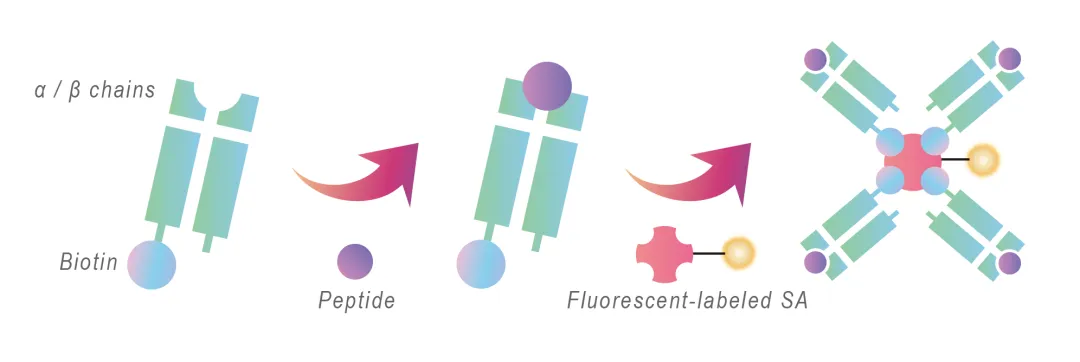
MHC四聚体是由四个主要组织相容性复合体(MHC)分子通过核心链霉素亲和素系统组装而成的大分子复合物,每条MHC分子可呈递一段特定的抗原肽。该复合物携带荧光标记,能够通过流式细胞术或显微镜技术,实现对特异性T细胞受体(TCR)的高亲和力结合和可视化追踪。
在卵巢癌研究中,研究人员通常选择肿瘤相关抗原(TAAs)(如NY-ESO-1、 survivin、TP53突变体等)或新抗原(neoantigens)作为肽源,构建肽-MHC复合物。这些四聚体可准确识别患者外周血或肿瘤浸润淋巴细胞(TILs)中具有抗肿瘤潜能的T细胞克隆,为后续的免疫监测和治疗评估提供定量依据。
MHC四聚体在卵巢癌研究中能解决哪些关键问题?
当前卵巢癌免疫治疗面临的一大瓶颈是缺乏高度特异性的生物标志物和治疗靶点。MHC四聚体技术恰恰填补了这一空白:它不仅可以定量评估T细胞应答的频率和强度,还能鉴定T细胞识别的具体抗原表位。例如,在基于个体化新抗原的疫苗临床试验中,研究人员使用定制四聚体证实了疫苗诱导的T细胞克隆确实能够识别并杀伤患者自身的肿瘤细胞。
此外,该技术还有助于解析肿瘤微环境中的免疫抑制机制。通过对比不同疾病阶段或治疗响应者与非响应者中抗原特异性T细胞的数量和功能状态,可揭示免疫逃逸的关键环节,如T细胞耗竭或调节性T细胞(Treg)的干扰。

如何构建卵巢癌特异性MHC四聚体?面临哪些技术挑战?
构建卵巢癌特异性的MHC四聚体,首先需明确目标抗原。常见策略包括利用生物信息学预测高亲和力的MHC结合肽,或通过质谱分析直接鉴定卵巢癌细胞表面MCI分子所呈递的天然肽段。随后,通过体外重折叠技术将肽段与MHC分子结合,并借助生物素-链霉亲和素系统完成四聚体聚合。
然而,该技术仍存在多项挑战。第一,MHC分子的多态性要求必须使用与患者HLA分型完全匹配的等位基因分子,而卵巢癌患者人群的HLA多样性较高,使得广谱应用成本较大。第二,某些肽段与MHC的结合稳定性较差,导致四聚体信号微弱或假阴性率高。第三,低频T细胞(如针对罕见新抗原的T细胞)在样本中难以检测,需结合体外扩增或更灵敏的检测方法。
MHC四聚体技术如何与其他免疫分析手段协同应用?
单靠四聚体染色并不能完全揭示T细胞的功能状态,因此多参数流式细胞术、单细胞测序及胞内因子染色等技术常与之联用。例如,在分离出抗原特异性T细胞后,可进一步分析其表型(如CD8+/CD4+、记忆亚型、耗竭标志物PD-1、TIM-3等)、功能(IFN-γ、TNF-α、颗粒酶B分泌)以及TCR序列多样性。这类多维度分析不仅能够评估T细胞的抗肿瘤潜力,还可为个体化免疫组合策略提供依据,比如确定哪些患者更适合PD-1/PD-L1阻断疗法,或哪些抗原更适合作为疫苗靶点。
该技术在卵巢癌临床治疗中有何应用前景?
随着个体化医疗时代的到来,MHC四聚体技术正逐步走向临床转化。它可用于监测治疗性疫苗、T细胞回输方案(如TIL或CAR-T疗法)以及免疫检查点抑制剂等的疗效。例如,在治疗过程中动态追踪特异性T细胞克隆的扩增情况,可为疗效评估提供早期指标。此外,基于四聚体分选获得的T细胞可用于下一代T细胞疗法的开发。这些高度特异性的T细胞克隆经过扩增和功能优化后,回输至患者体内有望实现更精准、更持久的抗肿瘤效果。
结论:MHC四聚体是否是推进卵巢癌免疫治疗的关键技术?
综上所述,MHC四聚体技术通过精准识别抗原特异性T细胞,为卵巢癌的免疫机制研究、治疗策略优化及临床疗效评估提供了不可替代的工具。尽管其在标准化、成本控制和灵敏度方面仍面临挑战,但随着多重四聚体panel、微流控单细胞技术等新方法的发展,这一技术有望更广泛地应用于科研和临床环境,最终推动卵巢癌免疫治疗走向精准化和个体化。
未来,我们是否能够看到基于MHC四聚体分选的T细胞疗法成为卵巢癌常规治疗的一部分?这一问题仍需更多基础与临床研究的支持,但毋庸置疑的是,该项技术已经为我们打开了探索肿瘤-免疫相互作用的一扇重要窗口。













