- 最新进展
- 产品信息
引言:为什么说MHC是适应性免疫的“分子桥梁”?
主要组织相容性复合体(MHC)最初因其在器官移植排斥中的作用而被发现,但随着免疫学的发展,我们逐渐认识到其更根本的功能是参与抗原呈递。MHC分子可分为I类、II类和III类,其中I类和II类糖蛋白在细胞表面形成复合体,能够结合抗原肽段并将其呈递给T细胞,从而启动特异性免疫应答。这种机制不仅帮助区分“自我”与“非我”,也在感染、肿瘤及自身免疫病中发挥关键作用。
MHC多肽复合体的基本结构是怎样的?
MHC分子在结构上具有显著保守性,其肽结合区域形成一个开放的“凹槽”结构,可容纳约8–20个氨基酸长度的肽段。MHC I类分子由一条多态性α链和非多态性β₂微球蛋白非共价结合而成,其凹槽两端封闭,适合结合较短肽段(通常为8–10个氨基酸);MHC II类分子则由α链和β链共同组成,凹槽两端开放,可容纳更长的肽段(通常为13–25个氨基酸)。这种结构差异决定了两类分子在抗原来源和呈递对象上的分工。
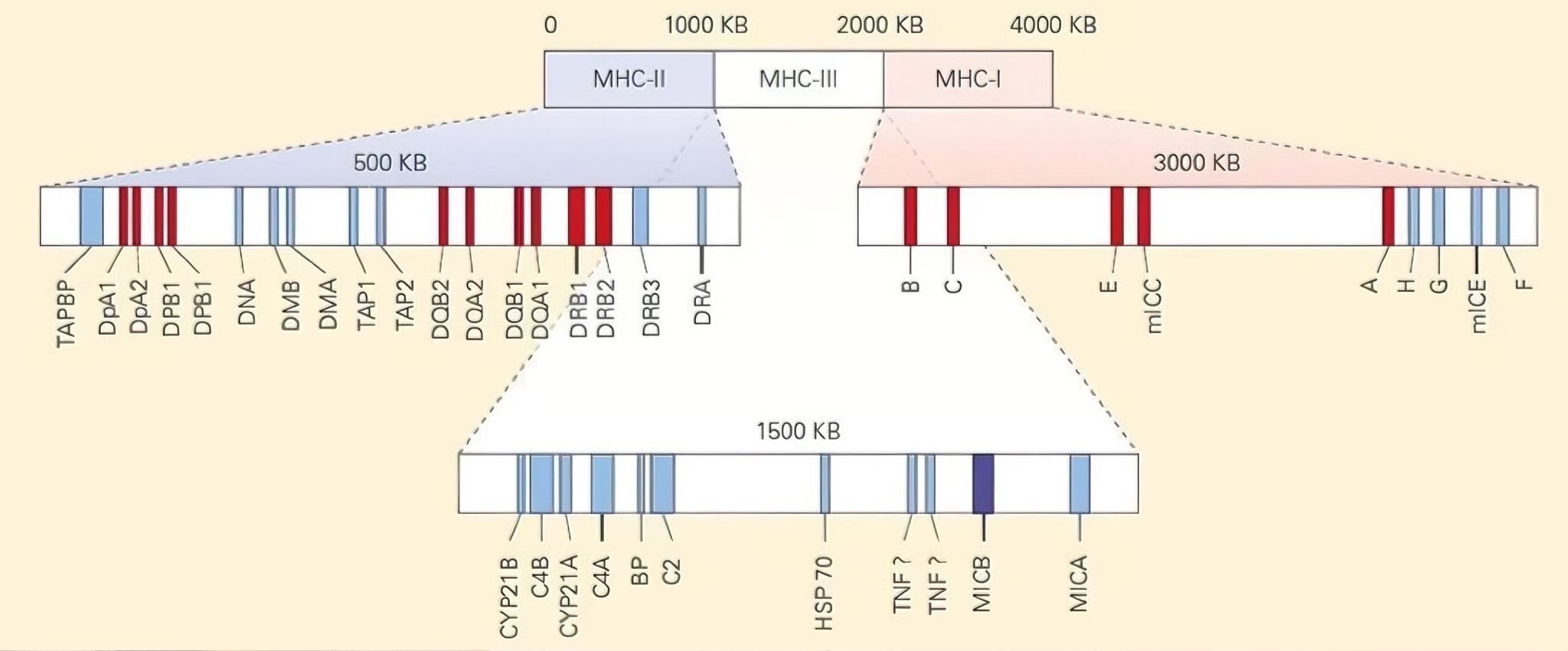
MHC分子如何实现其极高的多样性与肽段结合特异性?
MHC基因群具有多基因性和高度多态性。人类MHC(即HLA复合体)位于6号染色体短臂,包含超过200个基因,其中经典I类基因(HLA-A, B, C)和II类基因(HLA-DR, DQ, DP)呈现极丰富的等位基因变异。例如,目前已知HLA-B位点就有超过4800种等位基因。这种多样性使得不同个体所表达的MHC分子在肽结合凹槽的电荷分布和空间构象上存在差异,从而能够结合并呈递种类广泛的多肽,极大增强了群体水平的病原体应对能力。
内源性与外源性抗原的呈递路径有何不同?
根据抗原来源的不同,MHC多肽复合体的形成路径分为内源性途径和外源性途径:
内源性抗原(如病毒蛋白或肿瘤抗原)在胞质中被蛋白酶体降解为短肽,经TAP转运蛋白进入内质网,与正在组装的MHC I类分子结合。随后,该复合体经高尔基体转运至细胞膜,供CD8⁺ T细胞识别。
外源性抗原(如胞外细菌或可溶性蛋白)被抗原呈递细胞(APC)内吞后,在内体/溶酶体中被酶解为肽段。与此同时,MHC II类分子在内质网中与恒定链(Ii)结合,以阻止过早与肽段结合。进入晚期内体后,Ii链被降解,仅在凹槽中残留CLIP短肽,其后由HLA-DM分子协助将其置换为抗原肽,最终复合体表达于细胞表面供CD4⁺ T细胞识别。
为什么MHC限制性是T细胞活化的关键?
T细胞只能识别与自身MHC分子结合的抗原肽,该现象称为MHC限制性。CD8⁺ T细胞通常识别与MHC I类分子结合的内源肽,而CD4⁺ T细胞则识别与MHC II类分子结合的外源肽。这种机制确保了免疫应答的特异性,同时防止了对自身正常细胞的攻击。MHC多态性进一步提高了群体中对病原体应答的多样性,使得某些个体因携带特定HLA等位基因而对特定感染或疾病更具抵抗力。
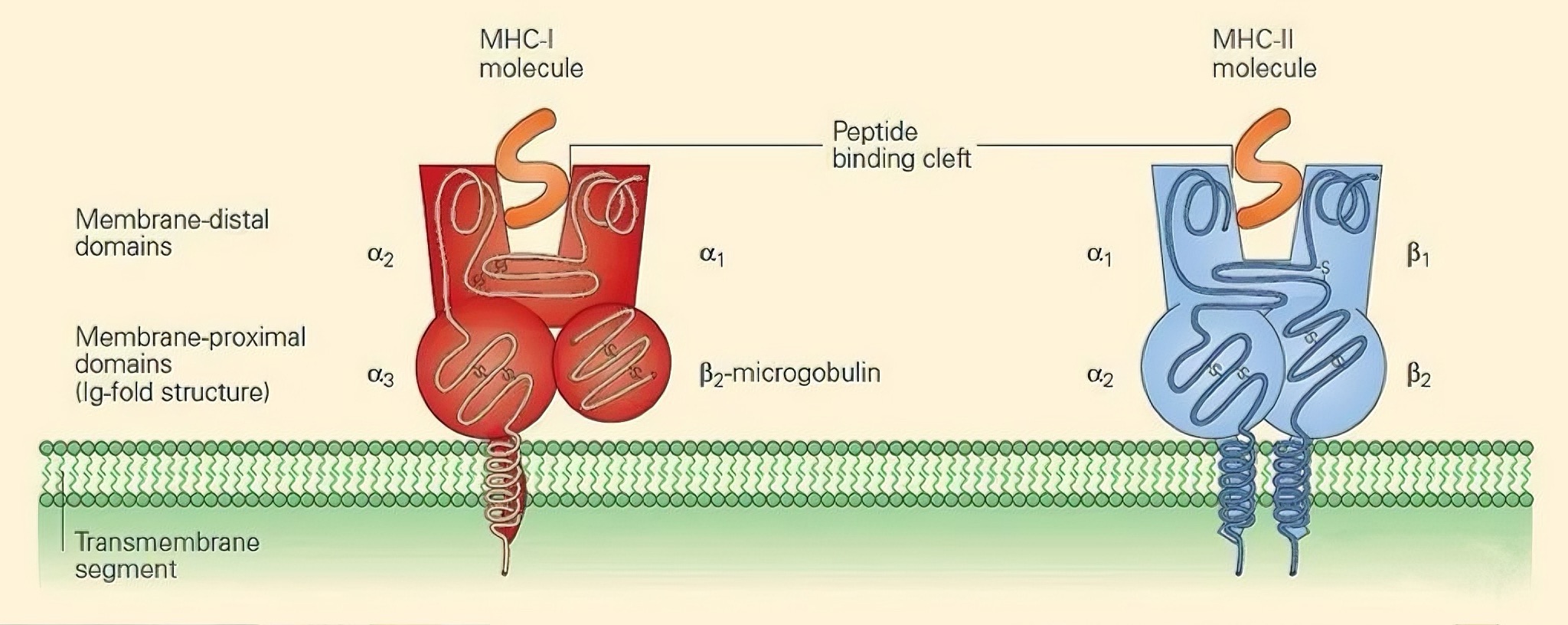
什么是连锁不平衡?它如何影响HLA分型与疾病研究?
连锁不平衡指不同MHC基因座上的等位基因在群体中非随机共同遗传的现象。例如,北欧人群中HLA-A01、B08、DRB1*03等位基因常以单倍型形式共同出现。这使得在器官配型或疾病关联分析中,可通过检测某一个基因座等位基因来预测其他座位的类型,提高了匹配效率和研究的可操作性。某些自身免疫病(如乳糜泻与HLA-DQ2/DQ8)和感染性疾病(如HIV控制与HLA-B*57)已被发现与特定HLA单倍型显著相关。
MHC多肽复合体在临床应用中有何价值?
基于MHC–多肽相互作用的机制,目前已发展出多项重要的临床应用:
疫苗设计:通过预测和筛选可与常见HLA分子高亲和力结合的病原体肽段,构建肽疫苗或m疫苗,增强T细胞免疫应答。
肿瘤免疫治疗:利用肿瘤特异性抗原肽(TSA)或肿瘤相关抗原(TAA)与自体M分子形成的复合体,体外扩增特异性T细胞后回输患者(如TCR-T疗法)。
自身免疫病诊断与干预:某些自身免疫病由特定HLA构象呈递自身抗原引发(如类风湿关节炎与HLA-DR4),可通过阻断相关MHC–肽复合物形成进行干预。
移植配型:HLA高分辩率分型可大幅降低移植物抗宿主病(GVHD)和排斥反应风险。
结语:MHC–多肽复合体研究将来何去何从?
尽管我们对MHC介导的抗原呈递机制已有深入理解,但该领域仍面临诸多挑战,例如非经典MHC分子(如HLA-E、G)的功能探索、MHC-I类分子交叉呈递机制的细化、以及个体化免疫治疗中MHC多肽复合体的精准设计等。结合结构生物学、多组学与人工智能方法,未来我们有望更全面揭示MHC在免疫应答中的调控网络,为新型疫苗和免疫疗法提供理论基石。













