MHC I 四聚体技术:抗原特异性T细胞研究的革命性工具
在免疫学研究中,如何精准地识别并分析抗原特异性T细胞一直是一个核心问题。细胞毒性T细胞(CTL)通过其T细胞受体(TCR)识别与MHC I类分子结合的肽段(pMHC),在抗病毒和抗肿瘤免疫中扮演关键角色。
- 最新进展
- 产品信息
MHC I 四聚体:如何革新抗原特异性T细胞研究?
在免疫学研究中,如何精准地识别并分析抗原特异性T细胞一直是一个核心问题。细胞毒性T细胞(CTL)通过其T细胞受体(TCR)识别与MHC I类分子结合的肽段(pMHC),在抗病毒和抗肿瘤免疫中扮演关键角色。但由于TCR具有极高的多样性——理论上可多达10²⁰种不同结构,传统的检测方法往往难以准确捕捉到特定的T细胞群体。直到1996年,Altman等人提出一项突破性技术——MHC I 四聚体,才真正为这一领域带来革命。
为什么我们需要MHC多聚体技术?
在免疫反应中,尤其是针对病毒感染或肿瘤发生的过程中,T细胞之所以能够识别并清除异常细胞,依赖于TCR对pMHC复合物的特异性结合。然而,单个pMHC与TCR的亲和力通常较低,这使得直接检测或分离抗原特异性T细胞极为困难。传统的细胞功能实验,如ELISpot或胞内因子染色,虽然能间接反映T细胞活性,却无法实现基于TCR特异性的直接标记和定量。因此,开发一种能够稳定结合TCR、并兼容多色荧光检测的工具,成为免疫学研究的重要目标。MHC多聚体技术应运而生,而其中最早问世且广泛应用的代表,正是MHC I 四聚体。
MHC I 四聚体是如何构建的?
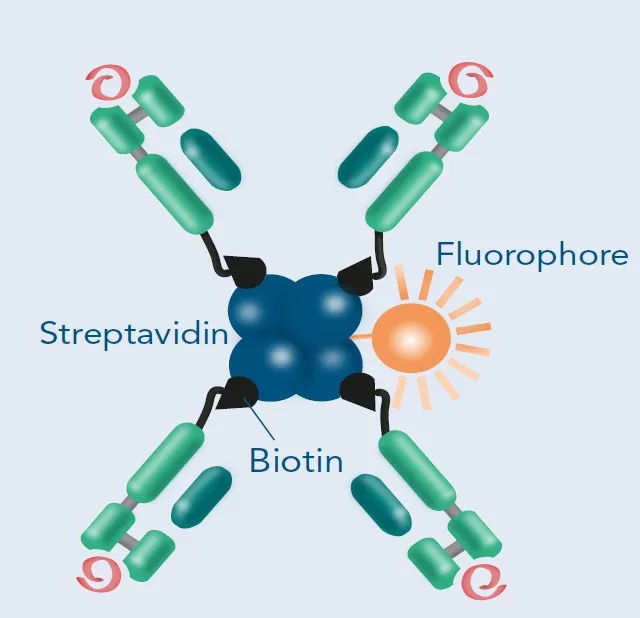
MHC I 四聚体的核心构造理念是通过多聚化增强结合亲和力。具体来说,每个四聚体由四个生物素标记的pMHC I单体分子与一个荧光标记的亲和素(Avidin)或链霉亲和素(Streptavidin)蛋白骨架结合而成。亲和素和链霉亲和素均可高效结合生物素,形成极为稳定的复合物。当这些pMHC分子以多价形式呈现时,其与T细胞表面TCR的结合强度大大增加,从而实现对特定T细胞的高效标记。研究人员只需通过流式细胞术,即可直接观察、定量甚至分选这些细胞。这种技术在病毒特异性T细胞研究、肿瘤免疫监测和疫苗评价中发挥了巨大作用。
四聚体技术之后,还有其他类型的MHC多聚体吗?
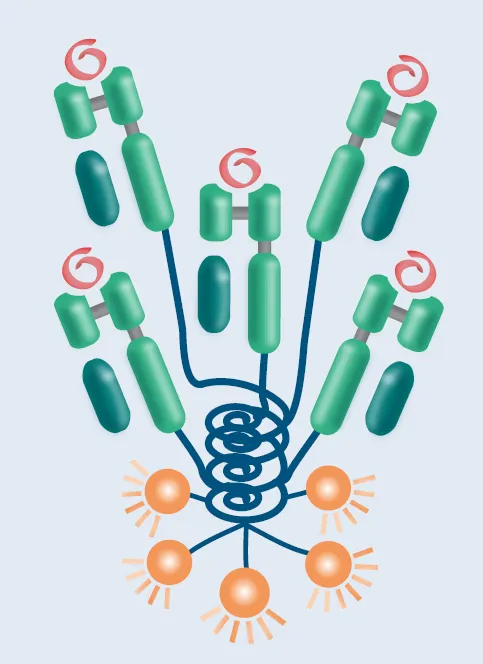
尽管四聚体技术奠定了MHC多聚体的基础,科学界并未停止对其进一步优化的探索。随着研究的深入,不同类型的多聚体相继被开发出来,以期在灵敏度、稳定性和功能性上实现突破。例如,五聚体(Pentamer)利用卷曲螺旋结构域组装五个pMHC分子,提升了荧光信号强度和结合亲合力;Streptamer和Dextramer则分别基于Strep-Tactin®-Tag系统或葡聚糖骨架实现多聚化,在保持高结合能力的同时拓展了应用的灵活性。值得注意的是,Streptamer技术还实现了可逆结合,通过添加生物素竞争性解离pMHC与骨架之间的连接,从而避免了对T细胞功能的干扰,为后续细胞功能实验提供了便利。
可逆性结合为何如此重要?
在多聚体技术的发展中,“可逆性”逐渐成为一个关键改进方向。传统的四聚体或五聚体在与T细胞结合后通常无法自然解离,这种不可逆的结合可能导致T细胞活化、内化标记复合物、甚至影响细胞存活和功能,使得后续实验难以开展。而可逆性多聚体(如Streptamer)通过添加竞争性小分子(如生物素或咪唑)能够主动解离pMHC复合物,恢复T细胞的天然状态。这一特性特别适用于需要回收活细胞进行扩增、功能分析或过继性转移的研究,例如在TCR-T细胞治疗开发过程中,可逆染色技术显著提升了细胞产品的可靠性和有效性。
MHC I 四聚体技术当前面临哪些挑战?
尽管四聚体技术自诞生以来已被广泛使用,它仍然存在一些局限性。除了上述不可逆性可能干扰细胞功能的问题外,四聚体对低亲和力TCR的检测能力有时仍显不足。此外,在多重染色或需要极高分辨率的复杂实验设计中,四聚体的信号可能与其他荧光标记发生冲突。近年来,多种新技术包括条形码编码多聚体、富集测序结合多聚体筛选等方案正在不断涌现,不仅弥补了传统方法的不足,也进一步推动了个性化免疫治疗和精准免疫监测的发展。
总结:四聚体技术的贡献与未来展望
自二十多年前问世以来,MHC I 四聚体技术不仅极大推动了基础免疫学的发展,也为临床研究和治疗提供了坚实工具。它是第一代能够在复杂细胞群体中直接标记抗原特异性T细胞的关键试剂,开辟了免疫监测和T细胞相关治疗策略的新天地。尽管新的多聚体类型持续演进,四聚体仍因其稳定性和成熟性在许多实验室中广泛使用。未来,结合蛋白质工程、单细胞技术和高通量筛选,多聚体技术有望在多特异性免疫应答解析和个体化医疗中扮演更加关键的角色。













