- 最新进展
- 产品信息
- 参考文献
1. IL-33是什么?在肿瘤微环境中究竟扮演什么角色?
IL-33是白介素1细胞因子家族的成员,最初被命名为DVS27。它在多种器官的组织屏障细胞中呈组成性表达,其特异性受体为致癌抑制因子2(ST2)。ST2作为IL-1受体样蛋白,迄今已鉴定出四种异构体,包括两种变异型(ST2LV和ST2V)、一种可溶性ST2(sST2)及一种膜结合型(ST2L)。ST2主要表达于造血细胞系和淋巴细胞系,尤其在辅助性T细胞中高度富集,并参与免疫系统调节。
作为一种多效性细胞因子,IL-33不仅是炎症的重要调节因子,可诱导Ⅱ型辅助性T细胞(Th2)介导的固有和适应性免疫反应,还在组织稳态维持、损伤修复以及免疫微环境重塑中发挥关键作用。由于其在炎症过程中表达显著上调,IL-33已被视为多种炎症性疾病及肿瘤进程中的潜在介质。本文将系统阐述IL-33在不同癌症类型中的表达特征及其复杂多样的生物活性。
2. IL-33在肿瘤发生中为何表现出“双重人格”?
随着研究的深入,IL-33/ST2信号通路被发现在肿瘤的发生、发展及预后判断中具有重要但往往矛盾的作用。其在常见恶性肿瘤如肺癌、乳腺癌和结直肠癌中均显示出抑癌与促癌的双重效应,具体作用取决于肿瘤类型、微环境背景及疾病阶段。
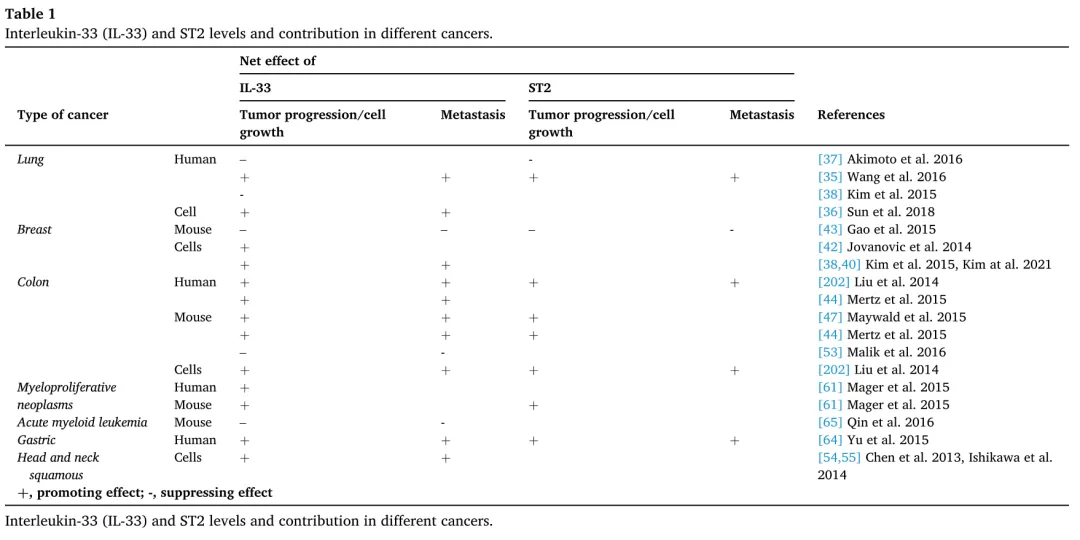
在肺癌中,一方面有研究指出IL-33/ST2轴可能促进肺纤维化与肺癌发生,使用IL-33抑制剂或上调sST2可能延缓纤维化进程;另一方面,也有证据表明IL-33可通过增强免疫细胞浸润与活化,进而抑制肿瘤转移与增殖。
在乳腺癌中,患者癌组织中IL-33或ST2的表达水平往往高于正常组织,提示其可能参与肿瘤进程;然而动物模型中IL-33过表达却显著抑制肿瘤生长与转移,显示出保护性作用。
在结直肠癌(CRC)中,情况同样复杂:部分研究发现IL-33/ST2信号可能促进肠道肿瘤发生,但也有研究指出ST2L在肿瘤组织中表达降低,且IL-33缺失可能影响B细胞调控,反而增加癌变风险。
此外,在其他癌种中,IL-33亦被报道仅发挥单向作用。这些相互矛盾的结论可能源于多方面因素:包括放疗、化疗对IL-33表达的扰动;人类与小鼠模型中的物种差异;IL-33给药剂量或遗传操控水平的差异;以及原代细胞与细胞系之间的生物学差异等。因此,在解析IL-33功能时,需综合考虑这些参数。
3. IL-33如何调控肿瘤微环境中的免疫细胞?
IL-33通过作用于多种免疫细胞,深刻影响肿瘤进程。其主要调控对象包括:
CD4⁺ T辅助细胞与调节性T细胞(Treg):IL-33/ST2信号可促进Th2型免疫反应,并在某些情境下扩增Treg细胞;但亦有研究显示其可能通过非ST2依赖途径诱导IFN-γ分泌,进而抑制肿瘤。
细胞毒性淋巴细胞:包括CD8⁺ T细胞和NK细胞。IL-33可通过增强这类细胞的效应功能,发挥抗肿瘤作用。
巨噬细胞:IL-33可促进其向M2型极化,增强肿瘤相关巨噬细胞(TAM)的免疫抑制功能。
髓源性抑制细胞(MDSCs):IL-33在不同肿瘤模型中可能促进或抑制MDSCs的扩增与免疫抑制活性,结果具有癌种特异性。
嗜酸性粒细胞与嗜碱性粒细胞:IL-33可直接或间接调节这些细胞的发育、活化及功能,进而影响抗肿瘤免疫或炎症反应。
Ⅱ型固有淋巴细胞(ILC2s):作为IL-33的关键靶细胞,ILC2s通过产生Th2型细胞因子,在肿瘤相关炎症与免疫调节中扮演重要角色。
4. 肿瘤微环境中哪些细胞来源的IL-33影响其功能?
IL-33在肿瘤微环境(TME)中的功能高度依赖于其细胞来源。基质细胞(如癌相关成纤维细胞CAFs)是IL-33的重要生产者,可通过调节免疫细胞募集及血管生成影响肿瘤进展;肿瘤细胞自身也可表达IL-33,直接调控细胞毒性免疫应答;此外,内皮细胞和上皮细胞来源的IL-33在某些癌种(如头颈鳞癌、黑色素瘤)中可能有利于抗肿瘤免疫。值得注意的是,不同细胞来源的IL-33可能通过改变局部免疫环境,最终对肿瘤发展产生相反的作用。
5. 哪些因素动态调控IL-33的活性与功能?
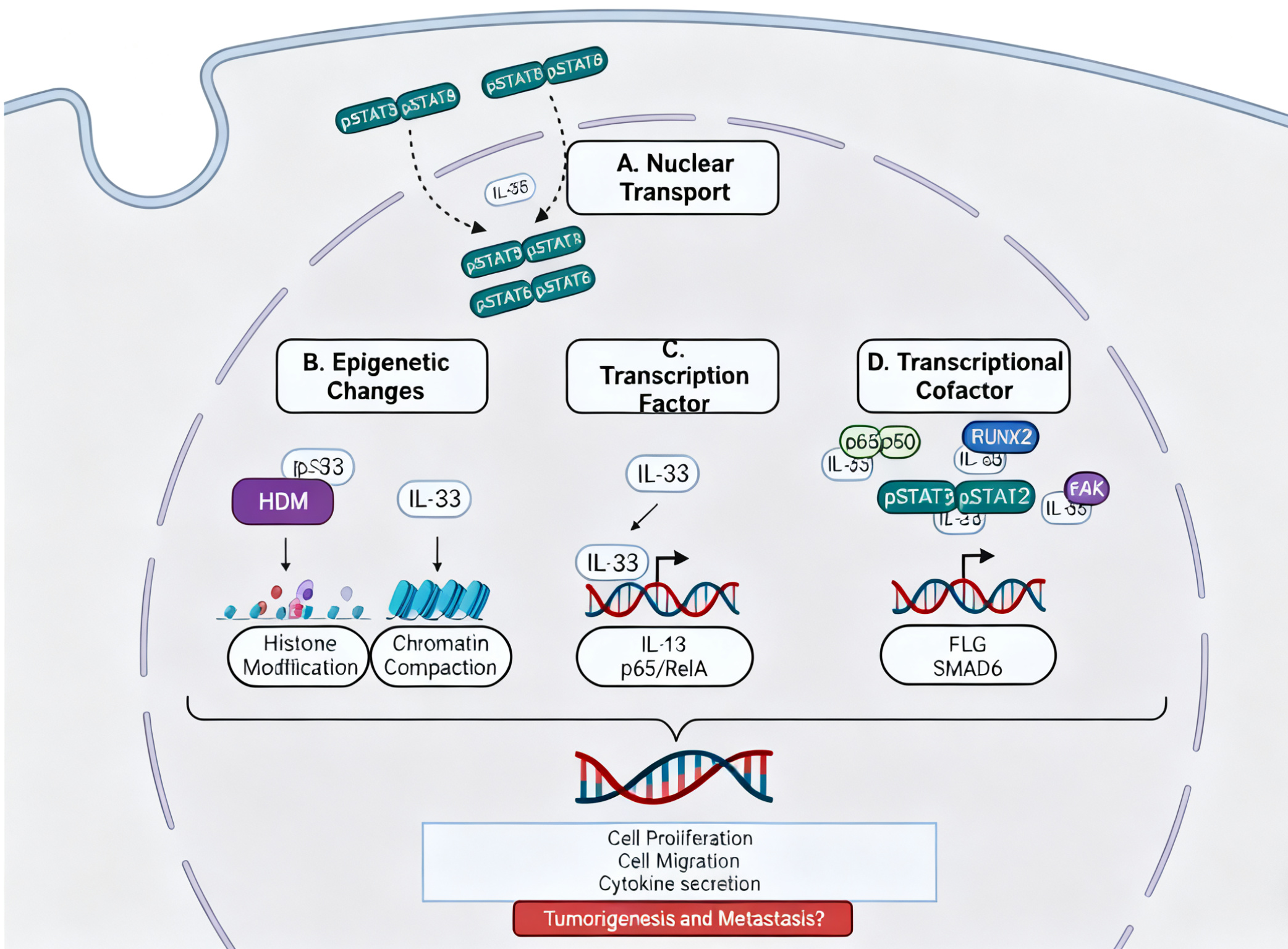
IL-33的表达和活性受到多维度动态调控。其不仅作为分泌型警报素行细胞外功能,还存在于细胞核内,可能通过调控NF-κB、JAK-STAT及SMAD等信号通路影响基因转录,进而参与肿瘤相关信号转导。此外,可溶性ST2(sST2)作为诱骗受体可拮抗IL-33/ST2L信号通路,甚至可能通过与未知受体结合发挥独立功能。这些复杂的调控机制是导致IL-33在肿瘤中功能报道不一致的重要原因。
6.未来关于IL-33的研究应聚焦哪些方向?
尽管IL-33/ST2轴在肿瘤免疫调节中的重要性日益凸显,其确切机制仍待阐明。未来研究应致力于厘清IL-33在不同肿瘤阶段、细胞来源及微环境背景下的具体作用机制,特别需要关注其核内功能与sST2的独立作用。通过多维度、多模型的研究策略,将有助于全面评估IL-33作为肿瘤诊断标志物和治疗靶点的潜力,并为开发新的免疫联合治疗策略提供理论依据。
[1] Yeoh WJ, Vu VP, Krebs P. IL-33 biology in cancer: An update and future perspectives. Cytokine. 2022 Sep;157:155961. doi: 10.1016/j.cyto.2022.155961. Epub 2022 Jul 14. PMID: 35843125.
[2] 张晓芙,颜上程,程馨仪,戴宇宁,伍诣娴,陈思嘉,朱一蓓.IL-33/ST2信号通路在肿瘤发生、发展和抗肿瘤免疫应答中的作用及其机制[J].现代免疫学,2022,42(03):236-242.
[3] 亓璐,苗玉辉,肖卫华,方芳.IL-33在肿瘤中的研究进展[J].生物学杂志,2018,35(05):1-7.
[4] 王海涛,卢斌峰,蒋敬庭.白介素-33对免疫细胞的影响及其作用机制[J].中国肿瘤生物治疗杂志,2021,28(05):526-530.
[5] 刘茜茜,陆地,胡嘉华,梁俊朝,陈火英.白细胞介素-33在肿瘤中的双重作用[J].中南大学学报(医学版),2021,46(02):169-175.
[6] 胡霞,单晶,孙晓滨.IL-33/ST2途径在肿瘤发生和发展中作用的研究进展[J].肿瘤预防与治疗,2019,32(04):366-371.













