免疫系统的“维和部队”:Tregs如何赢得2025年诺贝尔医学奖
北京时间2025年10月6日,诺贝尔生理学或医学奖授予美国科学家玛丽·E·布伦科、弗雷德·拉姆斯德尔和日本科学家坂口志文,以表彰他们在外周免疫耐受机制方面的开创性发现。
- 最新进展
- 产品信息
三位科学家历经30年的艰难探索,终于让免疫系统中这支曾被忽视的“维和部队”崭露头角,也为人类对抗自身免疫疾病和癌症开辟了全新的战场。
北京时间2025年10月6日,诺贝尔生理学或医学奖授予美国科学家玛丽·E·布伦科、弗雷德·拉姆斯德尔和日本科学家坂口志文,以表彰他们在外周免疫耐受机制方面的开创性发现。
他们的工作揭示了一个免疫系统的奥秘:我们之所以健康,不仅依赖于免疫系统强大的攻击能力,更依赖于一个同样强大的“刹车”系统——调节性T细胞。
01 免疫平衡的守护者:什么是Tregs?
在免疫学的漫长探索中,科学家们曾长期认为免疫力越强越好。然而,今年的诺贝尔奖揭示了一个反直觉的真相:健康的免疫系统不仅需要攻击力,更需要精准的调控能力。
调节性T细胞(Regulatory T cells,简称Tregs)正是一类专门负责抑制免疫反应的细胞,它们充当着免疫系统的“安全卫士”或“维和部队”。它们持续、主动地给免疫系统“踩刹车”,防止免疫系统错误地攻击自身组织。
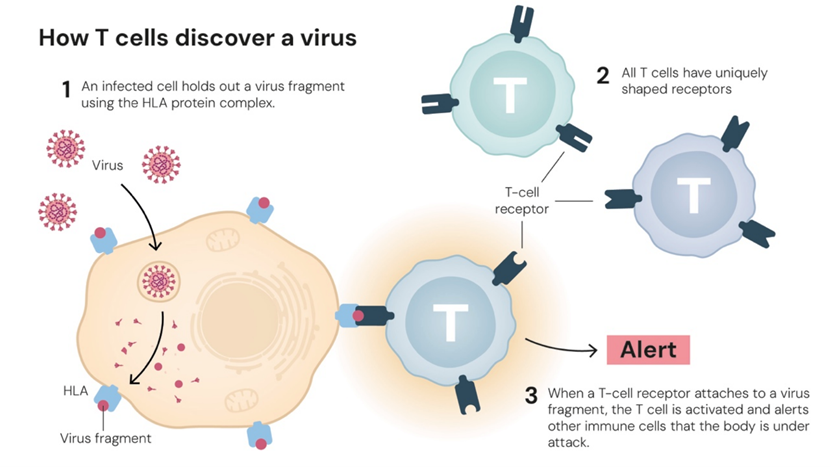
外周免疫耐受是指成熟的免疫细胞在人体外周免疫器官中对自身组织细胞或无害外来物质产生的无应答或低应答状态。其核心作用是防止成熟免疫细胞攻击自身组织引发自身免疫病,同时避免对无害物质过度反应。
02 从冷门到巅峰:Tregs的发现历程
这项诺奖级发现的诞生,是一部跨越30年的科学探索,其线索源自一个几乎被学界废弃的理论。在20世纪的大部分时间里,免疫学家们普遍认为,免疫耐受主要依赖于“中枢耐受”机制。胸腺作为免疫细胞的“训练学校”,会通过阴性选择的过程,清除那些可能攻击自身组织的T细胞。然而,总有一些“叛逆”的免疫细胞能够通过胸腺的筛选,进入外周循环系统。
坂口志文的坚持
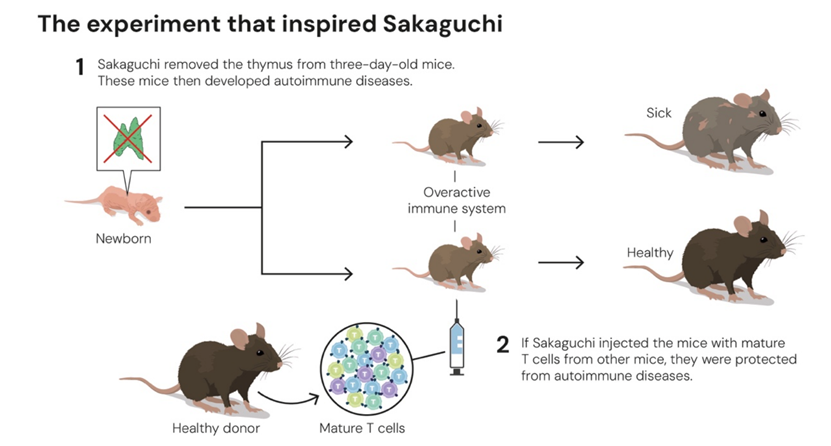
1995年,日本科学家坂口志文首次发现调节性T细胞。但这一发现初期因缺乏领域主流的支持而遭质疑、受冷遇。复旦大学基础医学院教授王继扬回忆,1990年,坂口志文在一次免疫学会议上报告有一种调节性T细胞,通过摘除胸腺清除这个细胞集团后,小鼠会发生自身免疫性疾病。现场没人相信,他讲完后也没有任何人提问。
基因层面的证据
转折发生在2001年,美国科学家布朗科与拉姆斯德尔在小鼠模型和人类遗传疾病中发现“Foxp3基因突变可引发致命性自身免疫病IPEX综合征”,且该突变所影响的关键免疫细胞正是Treg细胞。他们发现了一种名为“scurfy”的突变小鼠,这种小鼠会因免疫系统失控而早夭。经过数年艰苦的基因定位工作,他们找到了导致这一切的罪魁祸首——一个名为Foxp3的突变基因。
完美的结合
差不多同时,坂口志文也在小鼠上验证Foxp3基因是调节Treg细胞的关键转录因子。他们的研究形成“完美结合”,印证了Treg细胞在外周免疫耐受中的不可缺失的重要作用。2003年,坂口志文的团队将这两条线索联系起来,证明了布伦科和拉姆斯德尔发现的Foxp3基因,正是Tregs发育和功能的“主开关”。
03 免疫平衡的艺术:Tregs如何工作?
Tregs是T淋巴细胞中一个独特的小群体,仅占外周T细胞的5%-10%。它们通过多种方式维持免疫平衡。通常Tregs通过和进攻型T细胞“贴贴”或是分泌TGF-β、IL-10等抑制性细胞因子,让过度活跃的免疫反应踩刹车,从而诱导和维持免疫耐受。防止机体在清除病原或肿瘤后误伤自身组织。Treg功能在一定范围内波动,受到外界生理病理信号调控,对维持机体免疫稳态至关重要。
04 从实验室到病房:Tregs的临床应用
这一基础生物学发现正迅速转化为临床应用,为多种疾病的治疗提供了全新范式。
自身免疫疾病治疗
在类风湿关节炎、炎症性肠病和型糖尿病等自身免疫疾病中,问题在于免疫系统攻击过度。因此,治疗思路就是增强Tregs的功能或数量,为免疫系统“踩刹车”。目前,利用低剂量白细胞介素-2(IL-2)或直接输注在体外扩增的Treg细胞等策略,正在临床试验中被积极探索。
癌症治疗新方向
在癌症中,情况恰恰相反。狡猾的肿瘤细胞会“劫持”和招募大量Tregs作为自己的“保镖”,抑制其他免疫细胞对癌细胞的攻击。因此,抗癌的新思路就是暂时清除或抑制肿瘤内部的Tregs,为免疫系统“松开刹车”。
辉瑞、阿斯利康,都已经布局了CD25-ADC药物。复旦大学基础医学院应天雷/吴艳玲团队、王明伟团队也发表了相关研究进展:通过清除Treg细胞等,实现了80%的肿瘤消退。
器官移植及其他应用
从患者体内分离出调节性T细胞,并在实验室中扩增,随后将这些细胞重新返还到患者体内,从而增加调节性T细胞的数量。在某些情况下,研究人员还会改造这些T细胞,使其表面带有抗体,就像一个地址标签,这样,研究人员就能将这些“细胞安全卫士”精准送往移植的肝脏或肾脏,保护器官免受免疫系统攻击。
05 2025年诺贝尔生理学或医学奖与优爱的 Treg Polarization Kit, Mouse/小鼠Treg极化套装 的联系

基于诺贝尔奖的研究范式,您的Treg极化套装可以帮助您从以下几个方向深入探索免疫学的前沿问题:
- 进行机制研究:您可以利用该试剂盒产生的Treg,深入研究其抑制其他免疫细胞(如效应T细胞)活化的具体分子机制。
- 构建疾病模型:通过在体外生成Treg,并将其过继输入到疾病模型小鼠(如自身免疫性脑脊髓炎EAE模型、过敏性哮喘模型或移植模型)中,可以直观研究Treg在疾病中的治疗作用。
- 探索治疗策略:您的研究可以服务于治疗开发。例如,筛选能够促进Treg功能的小分子药物,或优化体外扩增Treg的方案,为细胞治疗 提供前期的数据支持。
希望各位老师能够带领优爱蛋白早日冲击诺贝尔奖!













