- 最新进展
- 产品信息
一、PROTAC技术概述:从抑制到降解的范式革命
传统的小分子药物和抗体药物大多通过“占据驱动”的模式发挥作用,即通过结合在靶蛋白的活性位点上来抑制其功能。这种模式面临诸多挑战,如难以靶向无明确活性位点的蛋白、易产生耐药性等。
PROTAC技术开创了一种全新的“事件驱动”模式,其工作机制是一个催化循环过程:
- 形成三元复合物:PROTAC分子同时结合目标蛋白和E3连接酶,形成一个短暂的POI-PROTAC-E3 Ligase三元复合物。
- 泛素化:E3连接酶将泛素链转移到目标蛋白上,将其标记为“待销毁”。
- 降解:被泛素标记的目标蛋白被细胞内的蛋白酶体识别并降解。
- PROTAC循环利用:PROTAC分子本身不被降解,可从复合物中解离,继续催化下一轮降解循环。
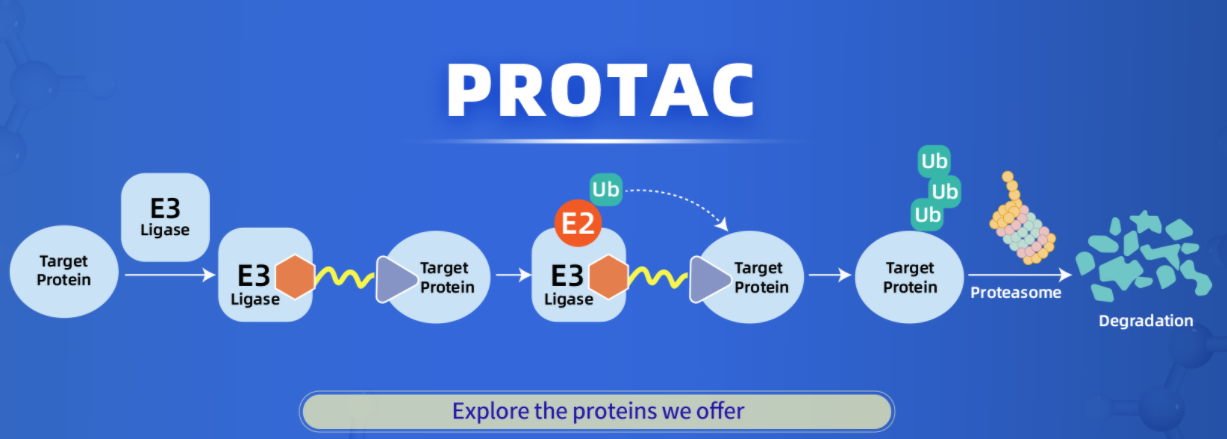
这种机制赋予了PROTAC技术高选择性、高效率和克服耐药性的独特优势,尤其适用于传统上被认为“不可成药”的靶点。
二、E3连接酶工具箱:PROTAC的“导航系统”
E3连接酶是PROTAC设计的核心,决定了降解的组织特异性、效率和安全性。人类基因组编码超过600种E3连接酶,但目前PROTAC开发中常用的仍局限于少数几种。
RING型 E3连接酶:种类最多,作为支架同时结合靶蛋白和E2泛素结合酶,直接催化泛素转移。
|
E3连接酶/复合物 |
特点与功能 |
在PROTAC中的应用 |
|
VHL 蛋白 |
冯·希佩尔-林道蛋白,一个氧感应蛋白复合物的组分。 |
PROTAC两大“明星”E3之一。与CRBN齐名,广泛用于PROTAC设计,已有多款招募VHL的PROTAC分子进入临床试验。 |
|
MDM家族 |
最重要的p53肿瘤抑制蛋白的负调控因子。 |
主要用于开发靶向MDM2本身的抗癌药物。也作为E3配体被用于降解其他蛋白的PROTAC中。 |
|
SCF 复合物 |
由Skp1, Cullin1, F-box蛋白组成。F-box蛋白(如β-TrCP, Skp2)负责底物识别,因此该复合物可降解多种底物。 |
是早期PROTAC设计的常用招募对象,但由于其复杂性,目前较少用。 |
|
APC/C 复合物 |
“后期促进复合物”,控制细胞周期进程,如降解细胞周期蛋白(Cyclins)。 |
主要在细胞周期中起作用,目前较少用于PROTAC设计。 |
|
Cbl 家族 |
主要负调控受体酪氨酸激酶,如EGFR、PDGFR等。 |
其配体可用于设计降解特定激酶的PROTAC,是一个有潜力的方向。 |
|
TRIM 家族 |
参与先天免疫、细胞分化等多种过程。 |
研究热点,正在探索其配体用于PROTAC,以开发免疫或抗病毒疗法。 |
|
β-TrCP |
识别含有特定磷酸化降解基序的底物,如β-Catenin, IκB。 |
作为SCF复合物的F-box蛋白,其识别机制被用于设计磷酸化依赖的PROTAC。 |
|
Skp2 |
识别并降解细胞周期抑制蛋白p27等,促进细胞增殖。 |
是癌症治疗的潜在靶点,也可作为E3配体来源。 |
|
IAPs |
凋亡抑制蛋白,通过抑制Caspase来阻止细胞凋亡。 |
其配体(如Bestatin类似物)被用于构建称为“SNIPERs”或“IAP-based PROTACs”的降解剂。 |
|
STUB1/CHIP |
与热休克蛋白协作,清除错误折叠的蛋白质。 |
在降解错误折叠蛋白(如与神经退行性疾病相关的蛋白)的PROTAC中具有潜力。 |
|
BRCA1-BARD1 |
BRCA1必须与BARD1形成异源二聚体才具有E3活性,在DNA损伤修复中起关键作用。 |
目前研究更多集中于其本身在癌症中的作用,在PROTAC中应用较少。 |
|
TRAF 家族 |
TNF受体相关因子,在免疫和炎症信号通路中起核心作用。 |
是免疫相关疾病PROTAC开发的潜在E3来源。 |
HECT型 E3连接酶:这类E3连接酶具有一个HECT结构域,其机制是先将泛素从E2“劫持”到自己身上,形成一个E3-泛素中间体,然后再将泛素转移到底物蛋白上。
|
E3连接酶/家族 |
特点与功能 |
在PROTAC中的应用 |
|
WWP 家族 |
包括WWP1, WWP2等,参与调控细胞生长、发育等过程。 |
其配体正在被探索用于PROTAC设计,以拓展可用的E3类型。 |
|
E6-AP |
由UBE3A基因编码,其突变与天使综合征相关。在HPV感染中,被病毒蛋白E6招募以降解p53。 |
是重要的神经生物学和肿瘤学靶点,其配体可用于PROTAC。 |
|
Smurf 家族 |
Smurf1和Smurf2,主要调控TGF-β信号通路和细胞极性。 |
在调控发育和细胞信号通路方面有潜力,但其PROTAC应用仍在探索中。 |
|
Itch |
调控免疫和炎症信号,如通过泛素化调控转录因子。 |
是一个有前景的E3,可用于设计免疫相关疾病的PROTAC。 |
|
HACE1 |
一个肿瘤抑制因子,通过降解Rac1等蛋白来抑制肿瘤生长。 |
研究相对较少,但因其底物与癌症相关而受到关注。 |
|
HUWE1 |
一个巨大的HECT型E3,降解多种底物,如Myc, p53, Mcl-1,在细胞命运决定中起核心作用。 |
由于其能降解多个关键致癌蛋白,是PROTAC开发中一个非常有吸引力的E3。 |
RBR型 E3连接酶:在机制上混合了RING和HECT的特点。它们有RING结构域来结合E2,但其催化机制类似于HECT型,会形成一个共价的E3-泛素中间体。
|
E3连接酶/复合物 |
特点与功能 |
在PROTAC中的应用 |
|
CRBN-DDB1 |
CRBN与DDB1等蛋白形成复合物,是沙利度胺及其衍生物(来那度胺、泊马度胺)的直接靶点。 |
PROTAC两大“明星”E3之一。绝大多数已进入临床的PROTAC都招募CRBN。其配体来自免疫调节药物,具有优异的药物性质和广泛的适用性。 |
|
Parkin |
与帕金森病密切相关,参与线粒体自噬(清除受损的线粒体)。 |
其配体被用于设计靶向线粒体相关蛋白的PROTAC,是神经退行性疾病治疗的研究热点。 |
|
HOIP/HOIL-1/LUBAC |
唯一已知的催化线性泛素链生成的复合物,对NF-κB信号通路至关重要。 |
其独特的线性泛素化功能正在被研究,以开发新型的PROTAC或调控工具。 |
|
HHARI |
与Parkin结构相似,参与转录调控和细胞应激反应。 |
研究仍在早期阶段,是拓展E3工具箱的潜在目标。 |
目前PROTAC研发严重依赖CRBN和VHL,这可能导致耐药性和组织特异性受限。未来发展的一个关键方向就是开发新型E3连接酶的配体,以扩充PROTAC的“工具箱”。
|
货号 |
产品名称 |
|
UA080262 |
Biotinylated CRBN/DDB1 Protein |
|
UA080011 |
DDB1/CRBN Complex, His Tag Protein |
|
UA080473 |
CRBN/DDB1 Protein, Dog |
|
UA080012 |
VHL/Elongin-C/Elongin-B Complex, His Tag Protein |
|
UA080162 |
MDM2 Protein |
|
UA085001 |
SKP1 His Tag Protein, Human |
|
UA085002 |
SKP2 GST Tag Protein, Human |
|
UA010573 |
XIAP(Bir3) His Tag Protein, Human |
|
UA070026 |
UBE3A His&Flag Tag Protein, Human |
仅展示部分产品,更多优质产品请联系我们~
三、热门靶点深度解析:PROTAC的“用武之地”
- STAT6
STAT6是信号转导与转录激活因子家族的重要成员,主要由IL-4或IL-13激活。它作为转录因子,在调节免疫反应、细胞分化和增殖等过程中发挥关键作用。STAT6在多种疾病中扮演重要角色,如特应性皮炎、哮喘和某些癌症。然而,STAT6功能缺失也可能导致免疫缺陷。
在STAT6靶点研究中,PROTAC技术展现出巨大潜力。通过降解STAT6,可从根源上解决相关疾病。例如,针对特应性皮炎的STAT6特异性PROTAC分子KT-621,已在临床试验中显示出快速降解血液细胞中STAT6的能力。
|
货号 |
产品名称 |
|
UA085003 |
Human STAT6/CRBN PROTAC Binding Kit |
|
UA080478 |
STAT6 His Tag Protein, Human |
|
UA080455 |
STAT6 (K595R) His Tag Protein, Human |
|
UA080456 |
STAT6 His-Strep Tag Protein, Human |
|
UA080457 |
STAT6 GST Tag Protein, Human |
- IRAK4
IRAK4是先天免疫的关键介质,其过度激活与多种自身免疫疾病相关。IRAK4不仅具有激酶活性,还作为支架蛋白参与信号传导。传统的小分子抑制剂只能阻断其激酶活性,无法干扰其支架功能,导致治疗效果受限。
针对IRAK4靶点的PROTAC降解剂能够同时阻断IRAK4的激酶活性和支架功能,更有效地抑制炎症信号通路。目前,全球已有多个IRAK4蛋白降解剂管线进入临床研究阶段,其中进展最快的是Kymera与赛诺菲合作开发的KT-474和国内药企领泰生物自主研发的LT-002。这些降解剂在治疗特应性皮炎和化脓性汗腺炎等疾病中展现出潜力。
|
货号 |
产品名称 |
|
UA080454 |
IRAK4 Protein, Human |
|
UA080294 |
IRAK4 His Tag Protein, Human |
- GSPT1
GSPT1是一种重要的翻译终止因子,通过识别mRNA上的终止密码子,促使翻译完成的蛋白质从核糖体中分离出来。在肿瘤细胞中,GSPT1的表达水平往往异常,其下调可导致关键蛋白的异常表达,进而抑制肿瘤细胞增殖或诱导凋亡。因此,GSPT1成为肿瘤治疗的潜在靶点。
GSPT1的降解可激活细胞的整合应激反应,导致细胞死亡。例如,GSPT1降解剂CC-90009在急性髓系白血病(AML)的临床试验中表现出良好的疗效。此外,GSPT1降解还被发现可以破坏白血病转录网络,降低关键融合蛋白及其相关转录因子的表达。
|
货号 |
产品名称 |
|
UA080159 |
GSPT1 GST tag Protein, Human |
- VAV1
VAV1是一种关键的信号转导蛋白,主要在造血细胞(如T细胞、B细胞等)中表达。VAV1通过其GEF(鸟苷酸交换因子)功能激活Rac/Rho家族GTPases,参与细胞骨架重组、细胞迁移与粘附、受体聚集与信号传导等过程。VAV1的异常表达或功能失调与多种疾病相关。在自身免疫和慢性炎症疾病(如类风湿性关节炎、炎症性肠病等)中,VAV1的异常激活可导致细胞因子过度分泌。在肿瘤中,VAV1的过表达与肿瘤的恶性程度、转移和预后密切相关。
近年来,VAV1作为PROTAC靶点的研究取得了显著进展。VAV1的降解可导致与免疫介导病症相关的细胞因子显著减少,因此在自身免疫和慢性炎症性疾病中具有潜在的治疗价值。例如,MRT-6160作为一种VAV1靶向的分子胶降解剂,在临床前和早期临床研究中表现出显著的疗效。
|
货号 |
产品名称 |
|
UA011223 |
VAV1 GST Tag Protein, Human |
|
UA080427 |
VAV1 GST Tag Protein, Human |
- IKZF1 / IKZF3
IKZF1(Ikaros)和IKZF3(Aiolos)是Ikaros家族的转录因子,具有高度保守的锌指结构,能调节淋巴细胞的分化、增殖。它们在多种免疫细胞中发挥关键作用,如在T细胞中调节白细胞介素2(IL-2)的表达。在肿瘤细胞中,IKZF1/IKZF3的异常表达与多种血液系统恶性肿瘤相关。
多个IKZF1/IKZF3靶向的PROTAC和分子胶降解剂已进入临床研究阶段。如CC-92480、CC-220(Iberdomide)和CC-99282等CELMoDs类化合物,在治疗复发/难治性多发性骨髓瘤(RRMM)和非霍奇金淋巴瘤(R/R NHL)中显示出良好的活性。此外,诺诚健华的ICP-490作为新型靶向蛋白降解剂,正在中国进行治疗多发性骨髓瘤的临床试验。
|
货号 |
产品名称 |
|
UA080160 |
IKZF1 GST Tag Protein, Human |
|
UA080161 |
IKZF3 GST Tag Protein, Human |
四、总结
PROTAC技术通过利用人体天然的蛋白降解系统,为疾病治疗开辟了前所未有的道路。随着对E3连接酶生物学理解的加深和药物化学技术的进步,针对STAT6、IRAK4等热门及难治靶点的PROTAC药物有望在未来十年内迎来爆发,真正实现从“不可成药”到“可降解”的跨越。













