- 最新进展
- 产品信息
最新进展
Siglec-2(又称 CD22)作为唾液酸识别免疫球蛋白样凝集素(Siglec)家族的高度保守成员,主要表达于 B 淋巴细胞表面,通过识别唾液酸修饰的糖链结构参与 B 细胞活化、增殖及耐受的精密调控。其独特的免疫调节功能使其在自身免疫病、B 细胞恶性肿瘤等疾病中成为关键调控分子,同时也为靶向治疗提供了重要靶点。本文系统阐述 Siglec-2 的分子特征、在免疫调控中的作用机制及其在疾病治疗中的研究进展。
一、Siglec-2 的分子特征与分型定位
Siglec-2 作为 Siglec 家族的经典成员,其结构特征与分型归属体现了功能的保守性与特异性。
(一)分子结构与分型特征
Siglec-2 属于 Ⅰ 型跨膜糖蛋白,隶属于 Siglec 家族中的高度保守型(与 Siglec-1、4、15 共同构成该亚群),其结构包含三个核心功能区域。胞外区由 7 个免疫球蛋白样结构域组成,其中 N 端第一个 V-set 结构域含唾液酸识别位点,可特异性结合 α2,6 - 连接的唾液酸残基(如 B 细胞表面糖蛋白 CD45 上的唾液酸化修饰),后续 6 个 C2-set 结构域负责维持蛋白构象与细胞间相互作用。跨膜区含一个带正电荷的赖氨酸残基,可与 B 细胞受体(BCR)复合物中的 Igα/Igβ 链相互作用,参与信号传导的调控。胞内区含 3 个免疫受体酪氨酸抑制基序(ITIM)和 1 个免疫受体酪氨酸转换基序(ITSM),当被 Src 家族激酶磷酸化后,可招募酪氨酸磷酸酶 SHP-1、SHP-2 及 SHIP-1,通过去磷酸化下游分子传递抑制信号。
这种结构使其兼具抑制性 Siglec 的典型特征,即通过 ITIM 介导的负反馈调节,避免免疫细胞的过度活化。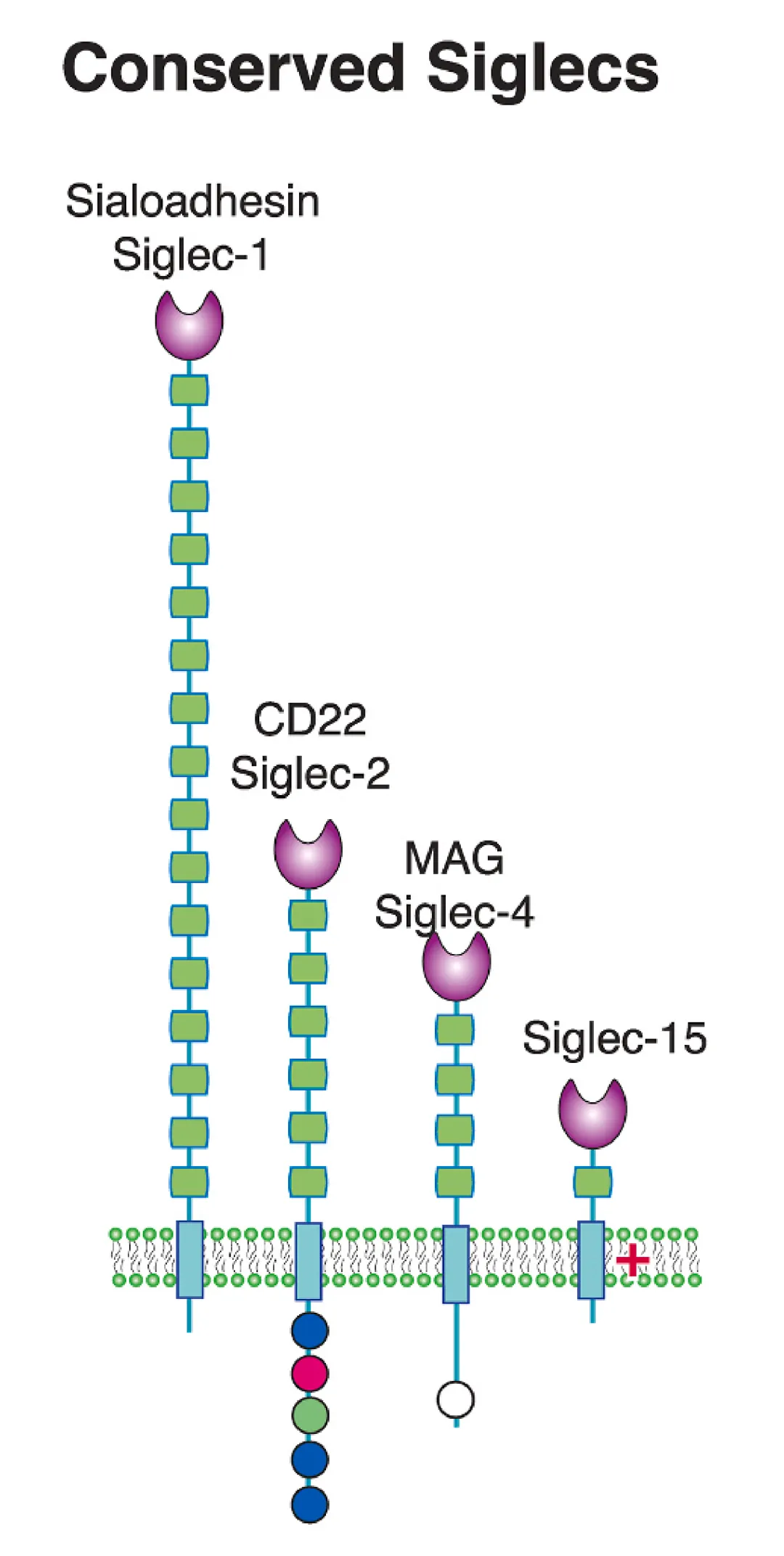

(二)组织表达谱
Siglec-2 的表达具有严格的细胞特异性。在 B 细胞发育的早期阶段(前 B 细胞)开始表达,在未成熟 B 细胞、成熟 B 细胞及记忆 B 细胞中持续高表达,而在浆细胞中表达显著下调,这种表达模式与 B 细胞的活化状态密切相关。在少数 T 细胞亚群(如调节性 T 细胞)及树突状细胞中存在低水平表达,但功能尚未明确;在唾液腺、肾脏等非免疫组织中也有少量检出,推测参与组织稳态维持。
这种限制性表达模式使其成为 B 细胞功能研究与靶向治疗的特异性标志物。
二、Siglec-2 在 B 细胞免疫调控中的作用机制
Siglec-2 通过与唾液酸配体的相互作用,在 B 细胞的活化、耐受及抗体分泌等过程中发挥核心调控作用。
(一)B 细胞活化的负反馈调节
B 细胞受体(BCR)介导的信号激活是 B 细胞应答的核心,而 Siglec-2 通过多重机制抑制过度活化。当 BCR 识别抗原并激活 Src 激酶(如 Lyn)时,Siglec-2 的胞内 ITIM 同时被磷酸化,招募 SHP-1/2,进而去磷酸化 BCR 下游的关键分子(如 Syk、PLCγ2),减弱钙内流与 NF-κB 通路激活,形成 “活化 - 抑制” 的动态平衡。配体依赖的调控机制同样重要:B 细胞表面的自配体(如唾液酸化 CD22、CD45)可通过 “顺式结合” 抑制 Siglec-2 的功能,而当 B 细胞与其他细胞(如树突状细胞)接触时,“反式结合”(如识别树突状细胞表面的唾液酸化配体)可增强其抑制活性,避免自身反应性 B 细胞的异常活化。
这种机制在维持 B 细胞耐受中至关重要,例如在中枢耐受阶段,未成熟 B 细胞通过 Siglec-2 识别骨髓基质细胞表面的自身抗原 - 唾液酸复合物,启动凋亡程序清除自身反应性克隆。
(二)B 细胞增殖与分化的调控
Siglec-2 通过影响细胞周期与细胞因子信号参与 B 细胞的命运决定。在 B 细胞受抗原刺激后,Siglec-2 的表达短暂下调,解除对增殖信号的抑制;当抗原清除后,其表达恢复,通过抑制 PI3K-AKT 通路终止细胞增殖,避免克隆过度扩增。在分化调节中,T 细胞依赖的 B 细胞分化过程中,Siglec-2 通过与 T 细胞表面 CD45 的相互作用,调控 IL-4、IL-5 等细胞因子的信号传递,影响浆细胞分化与 IgG1、IgE 的类别转换;在 T 细胞非依赖的应答中,则通过抑制 TLR 通路削弱 B1 细胞的抗体分泌。
研究表明,Siglec-2 缺陷小鼠表现出 B 细胞过度活化、血清自身抗体水平升高及生发中心异常增大,证实其在 B 细胞稳态中的关键作用。
三、Siglec-2 与疾病的关联及靶向治疗进展
Siglec-2 的功能异常与多种 B 细胞相关疾病密切相关,其特异性表达使其成为理想的治疗靶点。
(一)在 B 细胞恶性肿瘤中的作用
Siglec-2 在 B 细胞淋巴瘤、白血病等恶性肿瘤中持续高表达,成为疾病诊断与治疗的标志物。在慢性淋巴细胞白血病(CLL)中,肿瘤细胞表面的 Siglec-2 通过与自身唾液酸配体的顺式结合维持存活信号,同时通过反式结合抑制 NK 细胞的杀伤作用;在滤泡性淋巴瘤中,Siglec-2 的高表达与 BCR 信号亢进相关,促进肿瘤细胞的增殖与耐药。
靶向策略中,抗体药物偶联物(ADC)如 Inotuzumab ozogamicin,通过靶向 Siglec-2 将细胞毒性药物(卡奇霉素)递送至肿瘤细胞,已获批用于治疗复发 / 难治性 B 细胞急性淋巴细胞白血病(B-ALL),其疗效依赖于 Siglec-2 的内吞特性。双特异性抗体研究也在推进,针对 Siglec-2 与 CD3 的双抗可招募 T 细胞至肿瘤微环境,通过 T 细胞介导的细胞毒性杀伤肿瘤细胞,目前处于临床前研究阶段。
(二)在自身免疫病中的潜在价值
Siglec-2 的抑制功能缺陷可能导致自身反应性 B 细胞活化,参与类风湿关节炎、系统性红斑狼疮(SLE)等疾病的发生。SLE 患者 B 细胞中 Siglec-2 的表达下调,且其 ITIM 磷酸化水平降低,导致抑制功能减弱,自身抗体产生增加;小鼠模型中,Siglec-2 缺失可加剧狼疮样症状。
治疗探索方面,通过激活 Siglec-2 增强其抑制功能成为潜在策略,如使用 Siglec-2 的激动性抗体或唾液酸模拟物,在小鼠模型中可减少自身抗体分泌并缓解关节炎症,但临床转化仍需进一步研究。
(三)在感染性疾病中的作用
Siglec-2 可被病原体利用逃避免疫应答,同时也参与抗感染免疫的调控。某些病毒(如 EB 病毒)和细菌(如流感嗜血杆菌)可通过表达唾液酸化的表面蛋白,与 B 细胞表面的 Siglec-2 结合,抑制 BCR 信号,阻碍抗体产生。在细菌感染中,Siglec-2 通过识别细菌荚膜的唾液酸成分,调控 B 细胞产生特异性抗体,其表达水平与抗感染能力正相关,提示可通过调节 Siglec-2 功能增强疫苗的免疫原性。
四、研究挑战与未来方向
尽管 Siglec-2 的研究已取得显著进展,但其功能的复杂性与临床应用的挑战仍需深入探索。在分子机制层面,目前对 Siglec-2 识别的唾液酸糖链结构(如糖链长度、连接方式)与功能的关系尚未完全阐明,尤其是不同细胞表面配体(顺式 / 反式)如何调控其信号输出;同时,Siglec-2 与 PD-1、CTLA-4 等免疫检查点分子在 B 细胞中的协同作用机制,以及在肿瘤微环境中与 T 细胞、巨噬细胞的相互作用网络仍需解析。
临床转化的优化方向中,治疗安全性是关键问题,现有 ADC 药物可能导致正常 B 细胞损伤,引发免疫缺陷,需开发更具肿瘤特异性的靶向策略(如双靶点抗体)。联合治疗潜力巨大,Siglec-2 靶向治疗与 BCR 抑制剂、免疫检查点抑制剂的联合应用,可能增强抗肿瘤疗效,目前相关临床试验正在开展(如 NCT04855366 评估 Inotuzumab 与 CAR-T 细胞疗法的协同作用)。
结语
Siglec-2 作为 B 细胞特异性的抑制性受体,通过精细调控 B 细胞的活化与耐受,在免疫稳态维持中发挥不可替代的作用。其在 B 细胞恶性肿瘤中的特异性表达与功能异常,使其成为靶向治疗的重要突破口,已有药物在临床中展现出显著疗效。未来研究需进一步揭示其在复杂微环境中的调控网络,优化靶向策略,推动其在自身免疫病、感染性疾病等领域的临床应用,为免疫相关疾病的治疗提供新的理论依据与治疗手段。
声明:本篇文章在创作中部分采用了人工智能辅助。如有任何内容涉及版权或知识产权问题,敬请告知,我们承诺将在第一时间核实并撤下。
买重组蛋白,找南京优爱
优爱蛋白专注于提供药物研发、细胞治疗、基因治疗、基础科研所需各种蛋白类试剂原材料和服务,包括药物靶点蛋白、免疫检查点蛋白、细胞因子、工具酶、 蛋白定制表达、全长跨膜蛋白开发等。优爱致力于为客户提供优质的产品和专业服务,打造具有国际竞争力的高新技术企业。
靶点蛋白 | 膜蛋白 | 细胞因子 | 酶 | 病毒抗原 | 蛋白定制
南京优爱生物科技研发有限公司 邮箱:order@ua-bio.com 热线:0571-87565022

产品信息
©2021-2026 南京优爱生物科技研发有限公司版权所有
网站备案号 浙ICP备2022019033号-2 浙公网安备33010202004867号
电话:0571-87565022
邮箱:order@ua-bio.com
本网站销售的所有产品均不得用于人类或动物之临床诊断或治疗,仅可用于工业或者科研等非医疗目的。
- 0571-87565022
- order@ua-bio.com
-

联系我们











