- 最新进展
- 参考文献
在免疫学与疾病治疗领域,胸腺基质淋巴细胞生成素(TSLP)正成为一颗冉冉升起的新星。作为短链四α螺旋束Ⅰ型IL-2家族的多效性细胞因子,TSLP不仅在过敏性疾病和自身免疫性疾病中扮演关键角色,更在癌症、代谢综合征等复杂疾病中展现出独特的调控作用。其双重亚型结构、多细胞类型作用机制以及跨疾病谱的广泛影响,使其成为当前药物研发的热点靶点。
一、TSLP的生物学特性:从结构到功能的双重维度
TSLP存在长亚型(lfTSLP,159个氨基酸)和短亚型(sfTSLP,63个氨基酸)两种形式。长亚型通过Toll样受体(TLR2/3/6)配体、促炎细胞因子(IFN-γ、TNF-α)或病毒刺激诱导表达,与过敏性疾病、慢性炎症及癌症密切相关;短亚型则在多组织中稳定表达,参与免疫稳态维持。例如,在哮喘患者中,呼吸道病毒通过TLR3激活支气管上皮细胞,显著上调lfTSLP表达,而sfTSLP的合成可部分抵消其促炎效应。
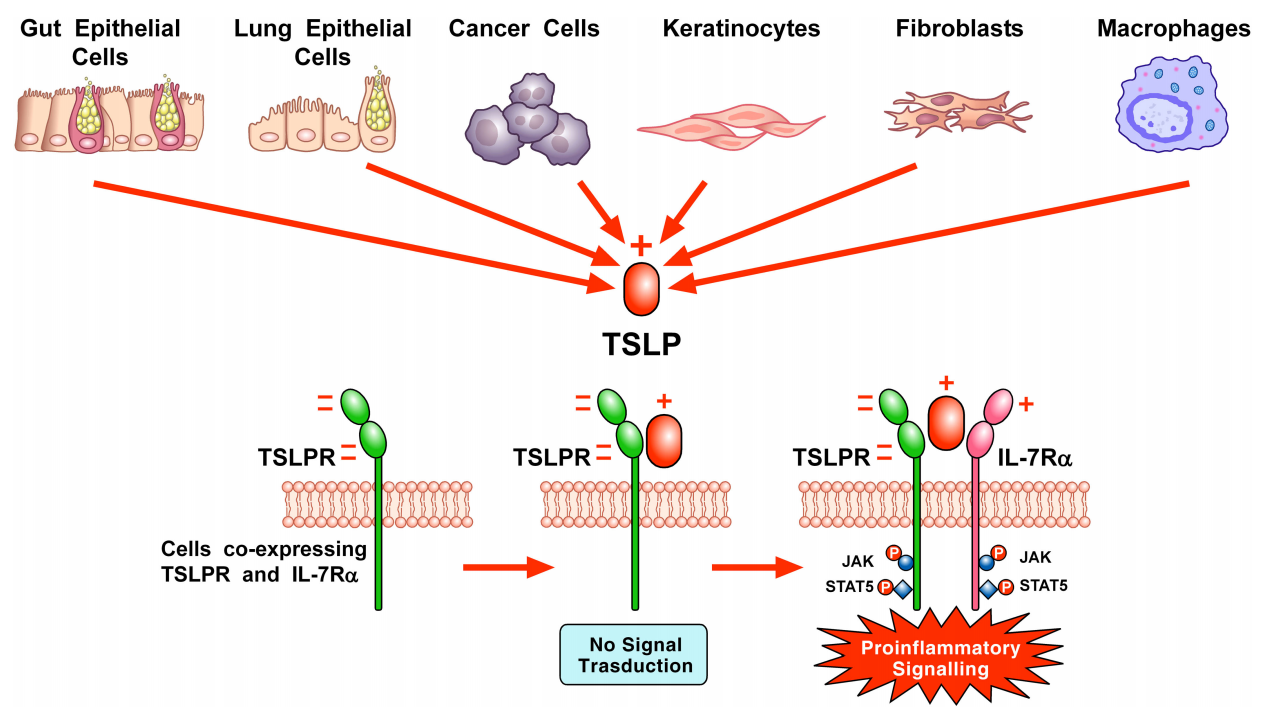
TSLP的受体复合物由TSLPR(胸腺基质淋巴细胞生成素受体)和IL-7Rα组成。当TSLP与TSLPR结合后,IL-7Rα的加入形成三元复合物,激活JAK1/JAK2-STAT5信号通路,驱动IL-4、IL-5、IL-13等促炎细胞因子的产生。这种机制使TSLP成为2型炎症反应的“总开关”——在哮喘中,它可直接促进树突状细胞(DC)成熟,诱导初始T细胞分化为Th2细胞;在特应性皮炎(AD)中,角质形成细胞释放的TSLP通过激活感觉神经元上的受体复合物,直接引发剧烈瘙痒。
二、临床转化:从哮喘到癌症的跨界突破
1. 哮喘治疗:首个无表型限制的生物制剂
TSLP在哮喘中的核心作用已通过全球首款抗TSLP单抗Tezepelumab(Tezspire)得到验证。该药物通过阻断TSLPR-TSLP-IL-7Rα三元复合物形成,显著降低哮喘急性发作风险。与传统生物制剂(如抗IgE、抗IL-5)仅针对特定表型(如嗜酸性粒细胞增多)不同,Tezepelumab适用于广泛重症哮喘患者,无论其表型或生物标志物状态如何。2023年,其全球销售额达5.67亿美元,预计2026年将突破20亿美元。
2. 特应性皮炎:瘙痒机制的新靶点
AD患者病变皮肤中TSLP表达量是正常皮肤的10倍以上。TSLP不仅通过激活DC驱动Th2免疫反应,还可直接刺激神经末梢产生瘙痒。目前,Tezepelumab正在开展针对中重度AD的Ⅲ期临床试验(NCT02525094),初步数据显示其可显著改善患者生活质量评分(DLQI)。国内企业如博奥信的Bosakitug(BSI-045B)也已进入AD的Ⅱ期临床,其差异化设计旨在提高药物在皮肤组织中的渗透性。
3. 癌症治疗:促癌与抑癌的双重角色
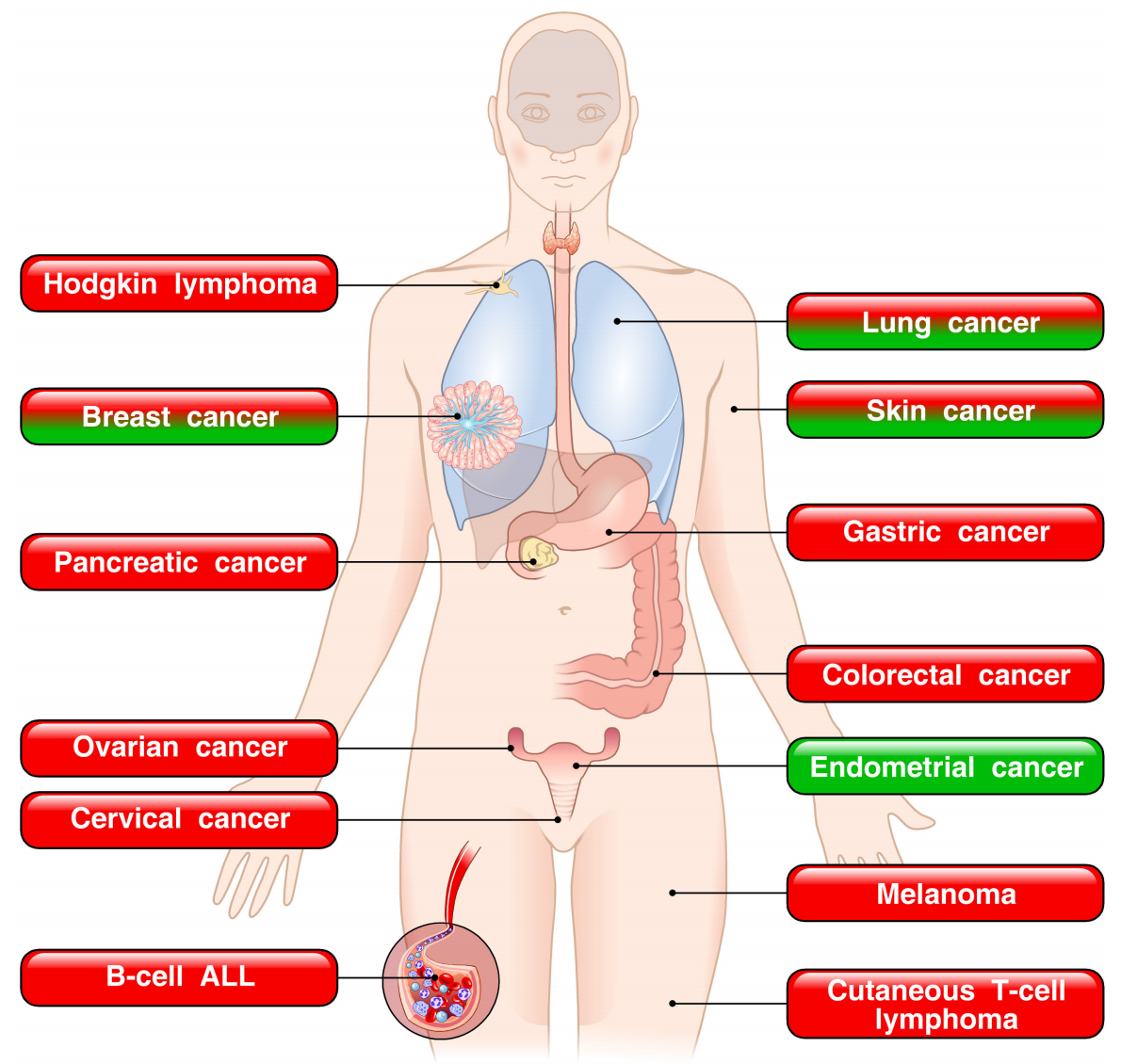
TSLP 在人类肿瘤中的双重作用。红色框表示已证实 TSLP 参与促进肿瘤生长的肿瘤类型。绿色框表示可能具有保护作用的肿瘤样本。混合的红色/绿色方框则表示在各种实验性癌症和人类癌症中,TSLP 兼具促进和抑制肿瘤生长的作用。
TSLP在癌症中的作用存在争议。例如在乳腺癌中,肿瘤细胞分泌的IL-1α通过诱导骨髓造血增加循环中性粒细胞数量,同时上调TSLP表达,促进肿瘤细胞存活;而在皮肤T细胞淋巴瘤中,TSLP可激活CD8+ T细胞直接杀伤肿瘤细胞。这种矛盾性可能与TSLP亚型差异有关——长亚型可能通过建立Th2型肿瘤微环境促进免疫逃逸,而短亚型可能通过维持免疫稳态抑制肿瘤进展。目前,针对TSLP的癌症治疗研究正聚焦于亚型特异性调控策略。
三、研发前沿:从单靶点到联合疗法的创新
1. 新一代抗体药物
安进/阿斯利康正在开发长效抗TSLP单抗AIO-001,其半衰期较Tezepelumab延长3倍,可实现每8周给药一次。国内企业如恒瑞医药通过license-out模式推进TSLP靶点研发,其授权给Aiolos的AIO-001全球权益已带来2150万美元预付款及超10亿美元里程碑付款。
2. 口服小分子抑制剂
针对TSLP信号通路的口服药物正在崛起。例如,TAK-279(口服TYK2抑制剂)在类风湿性关节炎(RA)Ⅱ期试验中,15mg组和30mg组分别有53.3%和54.2%的患者达到ACR20缓解标准,显著优于安慰剂组(29.2%)。这类药物可避免注射制剂的免疫原性问题,尤其适合基层市场。
3. 联合疗法探索
TSLP抑制剂与JAK抑制剂、IL-4/IL-13抑制剂的联用正在临床试验中。例如,Tezepelumab联合度普利尤单抗(抗IL-4Rα)在重度哮喘患者中的Ⅱ期试验显示,联用组年急性发作率较单药组降低42%,且未增加感染风险。
四、挑战与未来:精准医疗下的TSLP调控
尽管TSLP靶点前景广阔,但仍面临三大挑战:
亚型特异性调控:需开发区分lfTSLP和sfTSLP的检测技术与药物,避免“一刀切”式抑制导致的免疫稳态失衡。
跨疾病机制解析:例如,TSLP在妊娠期高血压疾病(如子痫前期)中表达下调,可能通过影响调节性T细胞(Treg)分化破坏母胎免疫耐受,但其具体机制仍需深入研究。
生物标志物开发:目前TSLP抑制剂的疗效预测仍依赖经验性用药,未来需建立基于基因多态性(如TSLP基因单核苷酸多态性rs1837253)或蛋白质表达水平的精准用药模型。
从哮喘到癌症,从单抗到口服药物,TSLP正以其独特的生物学特性重塑免疫相关疾病的治疗格局。随着对亚型功能、跨疾病机制及联合疗法研究的深入,这一“万能靶点”有望为更多患者带来突破性治疗方案。
相关产品推荐:
|
货号 |
品名 |
表达系统 |
|
HEK293 |
||
|
HEK293 |
||
|
HEK293 |
||
|
HEK293 |
相关文章推荐:
➷全球三大制药巨头围猎IL-33:谁能率先撞线COPD终点?
-
Remo Poto; Gianni Marone; Steven F. Ziegler; Gilda Varricchi. TSLP: contrasting roles in cancer. Frontiers in Immunology. 2025.
-
Steven F. Ziegler; David Artis. Sensing the outside world: TSLP regulates barrier immunity. Nature Immunology. 2010.













