小鼠Raw264.7与BMMs破骨分化:原理与应用指南
破骨细胞(Osteoclasts, OCs)是骨组织中唯一具有骨吸收功能的多核巨细胞,其分化与功能异常与骨质疏松、类风湿性关节炎、骨肿瘤等多种疾病密切相关。建立稳定、高效的破骨细胞体外诱导分化模型是骨代谢研究的基础。
- 最新进展
- 产品信息
破骨细胞(Osteoclasts, OCs)是骨组织中唯一具有骨吸收功能的多核巨细胞,其分化与功能异常与骨质疏松、类风湿性关节炎、骨肿瘤等多种疾病密切相关。建立稳定、高效的破骨细胞体外诱导分化模型是骨代谢研究的基础。
本文系统介绍了基于RANKL/M-CSF信号轴的两种经典破骨细胞诱导体系——RAW264.7细胞系诱导体系与原代骨髓单核细胞(BMMs)诱导体系,并重点介绍优爱生物(UA BIOSCIENCE)开发的配套细胞因子套装在两种模型中的应用方案,为骨生物学研究提供实验参考。
一. 破骨细胞分化的分子机制
破骨细胞来源于造血干细胞的单核-巨噬细胞谱系,其分化成熟受多种细胞因子精密调控。其中,巨噬细胞集落刺激因子(M-CSF)和核因子κB受体活化因子配体(RANKL)是破骨细胞分化最核心的调控因子:
M-CSF:通过与c-Fms受体结合,促进破骨前体细胞的存活、增殖和分化准备
RANKL:与破骨前体细胞表面的RANK受体结合,激活NF-κB、MAPK、PI3K/Akt等信号通路,驱动破骨细胞特异性基因(如NFATc1、TRAP、CTSK、MMP9等)表达,促进细胞融合形成多核成熟破骨细胞
体外实验中,通过外源性添加重组M-CSF和RANKL蛋白,可在细胞系或原代细胞中高效诱导破骨细胞分化。
二. 两种经典破骨细胞诱导体系比较
根据起始细胞来源的不同,破骨细胞体外诱导主要分为细胞系模型和原代细胞模型两大类,各有其适用场景和技术特点:
| 比较维度 | RAW264.7细胞系模型 | 原代BMMs模型 |
|---|---|---|
| 细胞来源 | 小鼠单核巨噬细胞白血病细胞系 | 小鼠骨髓原代单核细胞 |
| 操作难度 | 简单,无需分离原代细胞 | 较复杂,需骨髓冲洗和裂红处理 |
| 细胞均一性 | 高,细胞状态稳定 | 受个体差异影响 |
| 生物学相关性 | 适合机制研究 | 更接近生理状态 |
| 诱导效率 | 高,多核细胞比例大 | 中等,但功能更成熟 |
| 适用研究 | 药物筛选、信号通路研究 | 生理病理机制、药物评价 |
三. RAW264.7细胞系诱导破骨分化方案(UA090049)
操作流程:
1.破骨细胞前体细胞接种
1.1 将生长状态良好的Raw 264.7细胞用含10%胎牛血清(FBS)的α-MEM完全培养基重悬,并进行细胞计数。
1.2 将细胞以2.5 × 10³ cells/mL的密度,接种于已预先放置无菌盖玻片的24孔细胞培养板中,每孔加入1mL细胞悬液。
1.3 将培养板置于37°C、5% CO₂的细胞培养箱中静置培养18小时,使细胞充分贴壁。
2.破骨细胞诱导分化
2.1 细胞贴壁后(接种后约18小时),吸弃孔内旧培养基。
2.2更换为新鲜的破骨细胞诱导完全培养基。诱导培养基为含10% FBS的α-MEM培养基,并补充50 ng/mL重组小鼠M-CSF 蛋白及 100 ng/mL重组小鼠RANK L蛋白。
2.3此后,每3天更换一次诱导培养基。更换时,轻柔吸弃旧液,并加入等体积的、含有相同浓度M-CSF蛋白与RANK L蛋白的新鲜诱导培养基。
3. 细胞形态学观察与鉴定
3.1形态观察:自诱导开始,定期在倒置显微镜下观察细胞形态变化。通常,在RANK L诱导 4天 后,可观察到典型的多核破骨细胞样结构。
3.2 TRAP染色验证:RANK L诱导 5天 后,进行抗酒石酸酸性磷酸酶(TRAP)染色以特异性鉴定破骨细胞。严格按照TRAP染色试剂盒的说明书步骤进行染色操作。
染色完成后,在光学显微镜下观察。成熟的破骨细胞胞浆呈红色或红紫色。
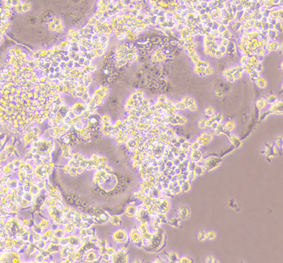
RANK L诱导 5天 后,显微镜下可观察到经典的多核破骨细胞结构
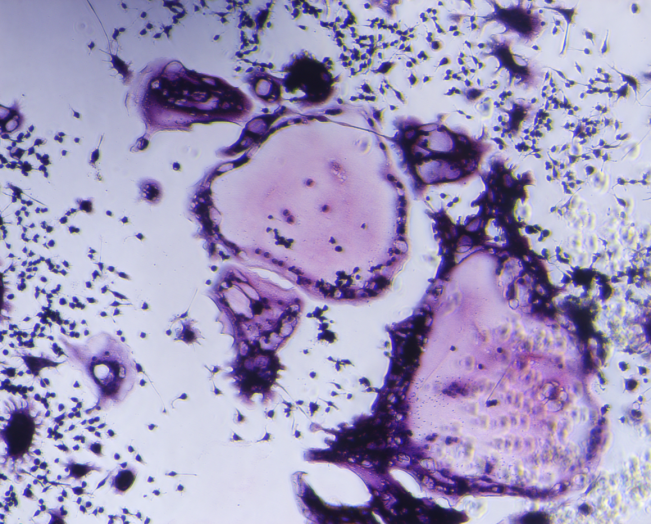
RANK L诱导 5天 后,进行抗酒石酸酸性磷酸酶(TRAP)染色以特异性鉴定破骨细胞。染色完成后,在光学显微镜下观察,成熟的破骨细胞胞浆呈红色或红紫色。
四. 原代骨髓细胞(BMMs)诱导破骨分化方案(UA090055)
操作流程:
1.骨髓细胞接种
1.1 将现取的小鼠骨髓细胞裂红后,用含10%胎牛血清(FBS)的α-MEM完全培养基重悬,并进行细胞计数。
1.2 将细胞密度稀释至2 × 10⁵ cells/mL,并加入M-CSF至终浓度为30ng/mL,细胞接种于已预先放置无菌盖玻片的24孔细胞培养板中,每孔加入1mL细胞悬液。
1.3 将培养板置于37°C、5% CO₂的细胞培养箱中静置培养5天,每2天换一次液(含30ng/mL M-CSF) 。
2.破骨细胞诱导分化
2.1 吸弃孔内旧培养基。阴性孔中加入含30ng/mL M-CSF的完全培养基,阳性孔中加入含30ng/mL M-CSF和50 ng/mL RANK L蛋白的完全培养基。
2.2此后,每2天更换一次培养基。阴性孔中加入含30ng/mL M-CSF的完全培养基,阳性孔中加入含30ng/mL M-CSF和50 ng/mL RANK L蛋白的完全培养基。
3. 细胞形态学观察与鉴定
3.1形态观察:自诱导开始,定期在倒置显微镜下观察细胞形态变化。通常,在RANK L诱导 4天 后,可观察到破骨细胞样结构。
3.2 TRAP染色验证:RANK L诱导 5-7天 后,进行抗酒石酸酸性磷酸酶(TRAP)染色以特异性鉴定破骨细胞。严格按照TRAP染色试剂盒的说明书步骤进行染色操作。
染色完成后,在光学显微镜下观察。成熟的破骨细胞胞浆呈红色或红紫色。
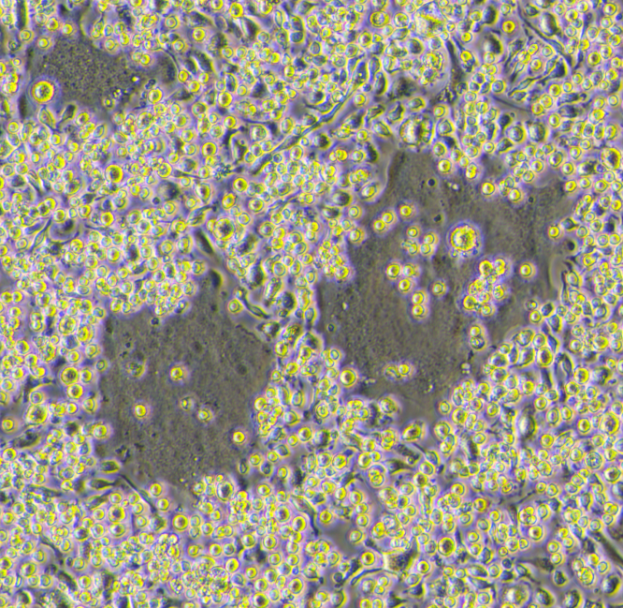
RANK L诱导 6天 后,显微镜下的破骨细胞。
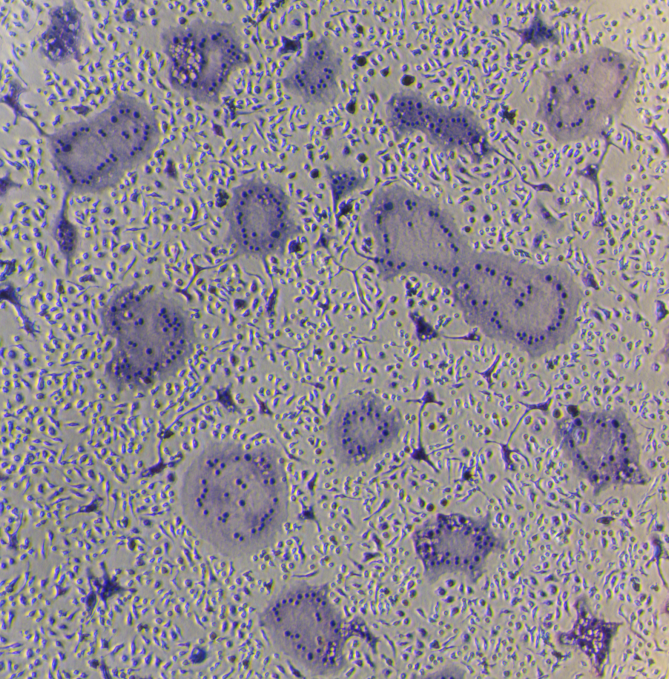
RANK L诱导 6天 后,进行抗酒石酸酸性磷酸酶(TRAP)染色以特异性鉴定破骨细胞。染色完成后,在光学显微镜下观察,成熟的破骨细胞胞浆呈红色或红紫色。
实验成功的关键控制点
要获得理想的诱导结果,除了严格按照说明书操作外,还需关注以下几个决定成败的细节:
细胞状态是基石。对于Raw264.7细胞,应使用低传代次数、对数生长期、状态饱满的细胞,传代时避免过度消化。
对于BMMs,无菌、快速、高效地分离小鼠股骨和胫骨中的骨髓细胞至关重要,并需彻底裂解红细胞以减少干扰。
试剂与操作的质量控制。重组细胞因子冻干粉溶解时,需使用无菌超纯水,并轻柔吹打混匀,避免反复冻融,建议分装保存。
在诱导过程中,换液动作需轻柔,避免将贴壁不牢的细胞(尤其是早期BMMs)吸走。全程使用经过验证的优质胎牛血清。
表型鉴定的金标准。显微镜下的多核形态是初步判断,TRAP染色是鉴定成熟破骨细胞不可替代的特异性方法。
染色后,成熟的破骨细胞胞浆应呈现鲜明的红色或红紫色,且细胞核不被染色。
五. 应用场景与研究展望
| 研究领域 | 推荐模型 | 应用示例 |
|---|---|---|
| 破骨分化机制研究 | BMMs模型 | 转录因子、信号通路调控研究 |
| 抗骨质疏松药物筛选 | RAW264.7模型 | 高通量筛选破骨分化抑制剂 |
| 天然产物活性评价 | 双模型验证 | 中药单体抗骨吸收活性研究 |
| 骨免疫微环境研究 | BMMs模型 | 炎症因子对破骨分化影响 |
| 基因功能研究 | RAW264.7模型 | 基因敲除/过表达效应分析 |
技术发展趋势
随着类器官技术和微流控技术的发展,破骨细胞体外模型正朝着三维培养、多细胞共培养(与成骨细胞、免疫细胞)、高通量自动化方向发展。UA BIOSCIENCE细胞因子套装的高活性和稳定性,为这些先进模型的建立提供了可靠的基础试剂保障。













