- 最新进展
- 产品信息
NIMA相关激酶7(NIMA-related kinase 7, NEK7)曾被视为细胞周期调控的"配角",如今却成为炎症性疾病和肿瘤治疗领域最受瞩目的新兴靶点之一。作为NLRP3炎症小体组装的关键"看门人"(gatekeeper),NEK7的靶向干预为应对从骨髓增生异常综合征到神经退行性疾病的广泛疾病谱系提供了全新策略。
NEK7是NEK(Never in Mitosis A)家族中最小的丝氨酸/苏氨酸蛋白激酶(分子量约35 kDa),与NEK6具有85%的结构同源性。与其他NEK家族成员不同,NEK7缺乏C端 regulatory 结构域,这使其在细胞周期调控中表现出独特的底物特异性。
经典功能:NEK7在有丝分裂期纺锤体组装检验点(spindle assembly checkpoint)中发挥核心作用,通过磷酸化动力蛋白(dynein)相关组分调控纺锤体极性和细胞质分裂。其异常表达与乳腺癌、结肠癌及非小细胞肺癌等多种实体瘤的发生发展密切相关。
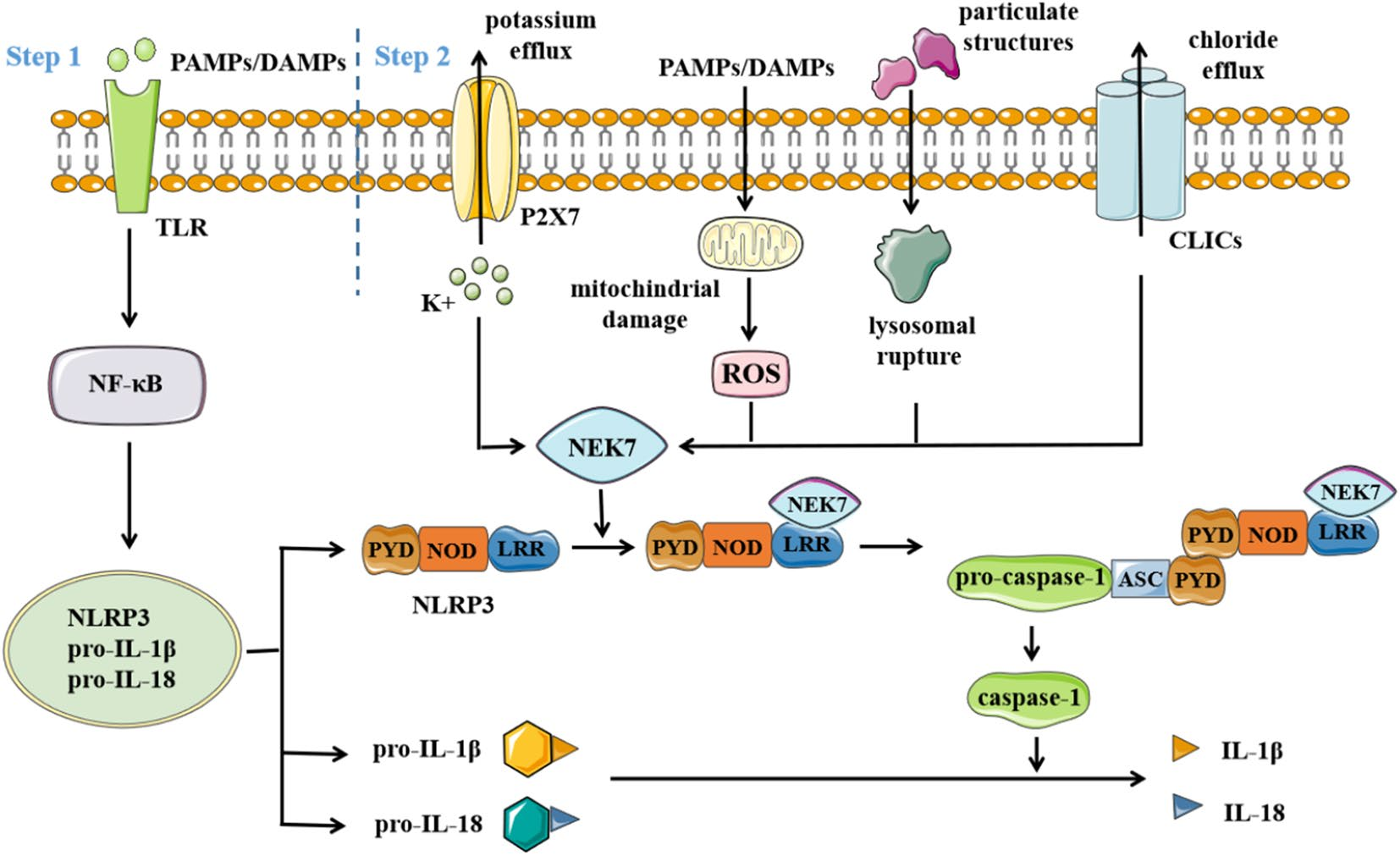
来源:doi.org/10.1007/s10787-022-01026-7
2019年Nature发表的结构生物学研究彻底重塑了科学界对NEK7的认知:NEK7是NLRP3炎症小体组装和激活的必需组分。在静息状态下,NEK7的低活性构象阻止NLRP3寡聚化;当接收到危险信号(如病原体相关分子模式PAMPs或损伤相关分子模式DAMPs)时,NEK7与NLRP3的LRR结构域结合,通过构象变化促进ASC招募及caspase-1激活,最终驱动IL-1β、IL-18的成熟释放及细胞焦亡(pyroptosis)。
这一发现将NEK7从细胞周期调控因子重新定义为先天免疫炎症通路的核心枢纽,开启了靶向NEK7治疗慢性炎症性疾病和炎症驱动型肿瘤的全新范式。
骨髓增生异常综合征(MDS)是与NEK7关联最为明确的适应症。低危MDS患者骨髓造血干/祖细胞中NLRP3炎症小体异常激活,导致IL-1β、IL-6、IL-8等促炎细胞因子持续释放,驱动无效造血、输血依赖及向继发性急性髓系白血病(sAML)转化。NEK7作为炎症小体组装的上游必需因子,成为阻断这一病理过程的关键干预节点。
复发性心包炎、动脉粥样硬化等心血管疾病的发病机制涉及IL-1β介导的慢性无菌性炎症。临床前研究显示,抑制NEK7可显著降低C反应蛋白(CRP)等心血管风险标志物,为口服靶向NLRP3通路的心血管保护策略提供了可能。
阿尔茨海默病(AD)、帕金森病(PD)等疾病的神经病理进程与神经炎症密切相关。中枢神经系统的NLRP3炎症小体激活驱动tau蛋白过度磷酸化和淀粉样蛋白沉积。NEK7抑制剂(尤其是具备血脑屏障穿透能力的分子)有望通过抑制神经炎症延缓疾病进展。
在2型糖尿病小鼠模型中,NEK7抑制显著改善代谢炎症(meta-inflammation)表型。肿瘤微环境研究发现,NEK7通过上调PD-L1表达促进食管鳞癌等实体瘤的免疫逃逸,与免疫检查点抑制剂联用可产生协同抗肿瘤效应。
当前NEK7靶向药物研发呈现"百花齐放"态势,多种技术路径并行推进:
Halia Therapeutics开发的Ofirnoflast是进展最快的NEK7靶向药物,也是全球首创(first-in-class)的口服变构抑制剂。其机制独特之处在于:
- 非竞争性抑制:结合NEK7的变构位点,阻断其与NLRP3的蛋白-蛋白相互作用(PPI),而非直接抑制激酶活性
- 促进解聚:不仅能阻止炎症小体形成,还能促进已组装炎症小体的解聚
临床进展(截至2025年11月ASH会议数据):
- 骨髓增生异常综合征(Phase 2):入组18例低危MDS伴症状性贫血患者,采用"5天给药+2天停药"的间歇给药方案(16周可延长至32周)。结果显示稳健且持续的血液学改善(HI-E),氧化线粒体DNA(mtDNA)及IL-8、IL-1β、IL-6等炎症标志物显著下降。FDA已授予孤儿药资格认定(Orphan Drug Designation)。
- 肥胖与2型糖尿病(Phase 2,NCT07172867):探索与司美格鲁肽(semaglutide)联合治疗,针对肥胖诱导的炎症性贫血。
- 阿尔茨海默病:早期临床试验阶段。
该药最大的临床优势在于精准靶向炎症小体而不引起广泛免疫抑制,规避了传统NSAIDs、糖皮质激素及IL-1生物制剂的脱靶毒性。
Monte Rosa Therapeutics开发的MRT-8102代表了靶向蛋白降解(TPD)技术在炎症性疾病领域的创新应用。作为NEK7选择性分子胶水降解剂,MRT-8102招募E3泛素连接酶cereblon,诱导NEK7泛素化及蛋白酶体降解。
关键临床前数据(2025年7月启动Phase 1):
- 在非人灵长类(NHP)模型中,口服给药5天使外周血单个核细胞(PBMCs)中NEK7蛋白水平降低85%,ex vivo LPS+nigericin刺激后IL-1β释放几乎完全抑制。
- 在肥胖人群(BMI>30)血液ex vivo模型中,抑制IL-1β的效力优于标准NLRP3抑制剂。
- GLP毒理学研究显示>200倍的治疗窗口(暴露量 margin)。
Phase 1试验(NCT07172867)设计包括单剂量递增(SAD)、多剂量递增(MAD)队列,以及针对高心血管疾病风险伴CRP升高患者的早期概念验证队列,初步结果预计2026年上半年公布。该技术路线的潜在优势在于事件驱动(event-driven)的药理作用:通过降解NEK7实现更持久、更深度的通路抑制,可能支持更低给药频率。
2024年发表的研究揭示,处于Phase III临床的抗癌药物Rociletinib(ROC)可共价结合NEK7的Cys79位点,阻断NEK7-NLRP3相互作用,在2型糖尿病小鼠模型中显著缓解代谢炎症。这一发现提示:
1. NEK7存在可成药的半胱氨酸口袋;
2. 已有临床安全性数据的药物可通过重定位(repurposing)快速进入NEK7相关适应症开发。
NEK7作为连接细胞增殖调控与先天免疫炎症的"分子桥梁",其靶向治疗开发代表了精准医学的重要方向。从2019年NLRP3-NEK7复合物晶体结构的解析,到2025年Ofirnoflast和MRT-8102相继进入临床关键阶段,短短六年间NEK7已从基础生物学发现快速转化为具有变革潜力的治疗靶点。
尽管面临蛋白-蛋白相互作用难靶性、血液学毒性管控等挑战,现有临床数据(尤其是MDS患者中观察到的血液学改善)已初步验证了靶向NEK7-NLRP3轴的治疗假设。随着Phase 2/3临床数据的积累和新一代降解剂技术的进步,NEK7抑制剂有望成为继JAK抑制剂、IL-1生物制剂之后,炎症性疾病和血液肿瘤治疗领域的重要新支柱。在2030年前,我们或将见证首个NEK7靶向药物获批上市,开启炎症精准治疗的新时代。













