- 最新进展
- 产品信息
从脂肪酸代谢到精准医疗的跨界突破:在代谢性疾病和恶性肿瘤的治疗领域,一个名为ACSL5(长链酰基辅酶A合成酶5)的分子正悄然成为制药界关注的焦点。作为脂肪酸代谢通路的关键守门人,ACSL5不仅调控着机体的能量平衡,更在肿瘤微环境、免疫调节和代谢综合征中扮演着多重角色。
靶点机制:细胞能量代谢的"交通指挥官"
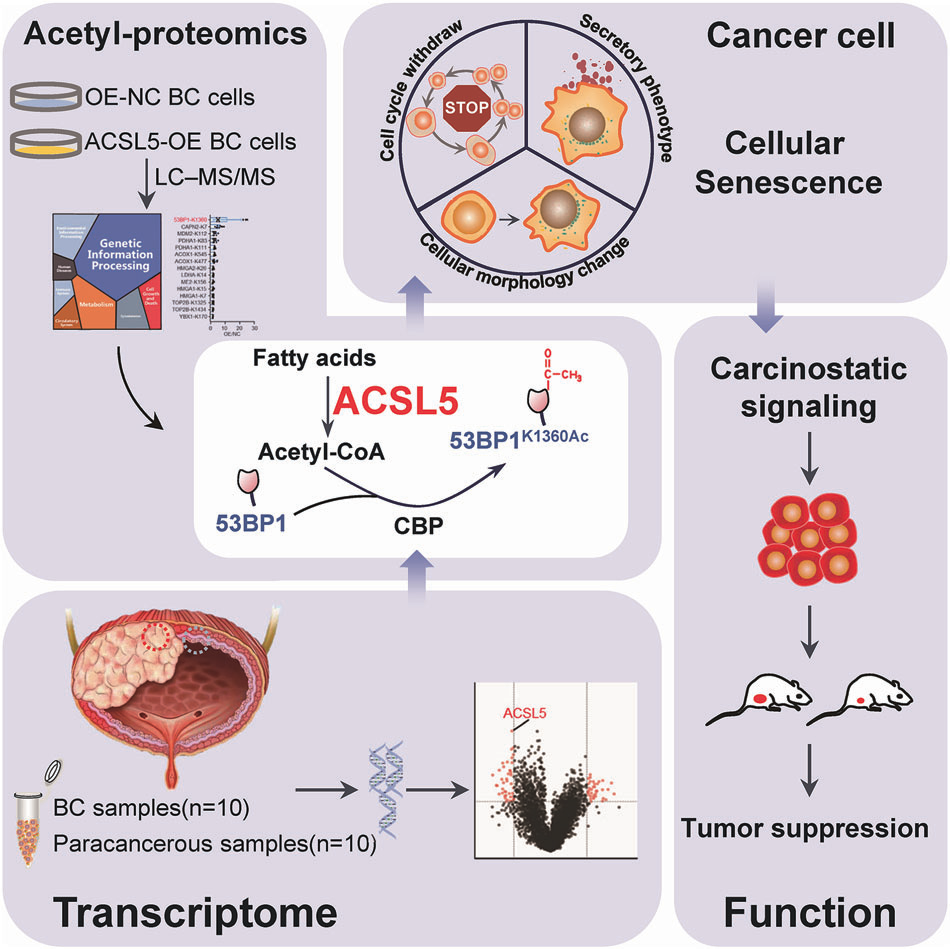
来源:Oncogene
ACSL5 促进脂肪酸氧化(FAO),减少细胞内脂质积累,同时增加乙酰辅酶A(Acetyl-CoA) 水平;乙酰辅酶A 促进蛋白质乙酰化从而诱导细胞衰老。
ACSL5属于长链酰基辅酶A合成酶家族,主要负责催化长链脂肪酸(C16-C20)与辅酶A结合,生成脂肪酸酰基辅酶A。这一看似简单的生化反应,实则是细胞能量代谢的分水岭:
- 脂质合成通路:生成的酰基辅酶A进入内质网,合成甘油三酯、磷脂等储存性脂质
- β-氧化通路:酰基辅酶A进入线粒体,通过氧化分解产生能量
- 信号转导:调控Wnt信号通路、细胞凋亡和炎症反应
ACSL5的独特之处在于其组织特异性表达——在肝脏、小肠、脂肪组织和骨骼肌中高度富集,使其成为调控全身代谢的理想靶点。
突破一:肥胖与代谢综合征的"刹车系统"
2024年重磅研究揭示,ACSL5是调控体重和代谢健康的关键开关。全球首个ACSL5基因敲除小鼠模型显示,缺失ACSL5的小鼠即使高脂饮食喂养,也能显著抵抗肥胖、胰岛素抵抗和脂肪肝的发生。
更令人振奋的是,研究团队成功开发出口服小分子ACSL5抑制剂LP-856866。该药物在饮食诱导的肥胖小鼠中展现出惊人的效果:
- 显著降低食物摄入量,持续28天
- 改善葡萄糖耐受性和胰岛素敏感性
- 降低血清甘油三酯和总胆固醇水平
- 关键优势:减脂同时最小化瘦体重流失
机制研究发现,ACSL5抑制通过激活回肠刹车机制(Ileal Brake)发挥作用——未完全吸收的游离脂肪酸刺激肠道L细胞释放GLP-1,延缓胃排空并产生饱腹感。这一发现为开发新一代减肥药物提供了全新思路。
突破二:肿瘤治疗的代谢干预新策略
在肿瘤领域,ACSL5展现出"双刃剑"特性,其表达水平与预后密切相关:
胰腺癌:预后标志物的新星
2019年发表于《OncoTargets and Therapy》的研究证实,ACSL5低表达是胰腺癌患者预后不良的独立危险因素。高表达ACSL5的患者无进展生存期显著延长,提示其具有抗肿瘤增殖作用。多变量分析显示,ACSL5表达水平与肿瘤分期、分化程度共同构成预后评估体系。
非小细胞肺癌:棕榈酸的抑癌媒介
2024年最新研究发现,在棕榈酸(C16:0)处理的非小细胞肺癌(NSCLC)细胞中,ACSL5是调控细胞增殖和迁移的主效调节因子。研究证实:
- 棕榈酸通过上调ACSL5表达抑制A549细胞增殖
- ACSL5敲除可阻断棕榈酸的抗肿瘤效应
- 机制涉及ERK信号通路的调控
值得注意的是,ACSL5在肺癌组织中的表达与增殖标志物Ki67呈负相关,进一步支持其抑癌作用。
联合治疗策略
针对ACSL家族广谱抑制剂Triacsin C的研究显示,ACSL5抑制可增强化疗药物吉西他滨和靶向药物吉非替尼的敏感性,为克服肿瘤耐药提供了新方案。
突破三:皮肤免疫与炎症性疾病
2025年4月发表于《Scientific Reports》的研究首次揭示ACSL5在红斑痤疮(酒糟鼻)中的关键作用。研究发现:
- ACSL5在红斑痤疮皮损中显著上调
- ACSL5与M1型巨噬细胞浸润密切相关
- 作为连接脂质代谢紊乱与先天免疫的"桥梁基因"
该研究提出,开发选择性ACSL5抑制剂可能成为治疗玫瑰痤疮的新策略,填补皮肤科靶向治疗的空白。
临床转化前景:从实验室到病床边的跨越
药物开发优势
- 成药性明确:ACSL5具有清晰的活性口袋,小分子抑制剂开发可行
- 安全性窗口:基因敲除小鼠未出现严重不良反应,提示治疗窗较宽
- 多适应症潜力:覆盖肥胖、糖尿病、非酒精性脂肪肝、肿瘤和炎症性疾病
在研管线动态
- LP-856866:首个进入临床前开发的ACSL5特异性抑制剂,已完成POC验证
- Triacsin C衍生物:针对ACSL家族广谱抑制剂的优化改造正在进行
- 靶向递送系统:利用ACSL5在肠道和肝脏的特异性分布,开发器官选择性药物
ACSL5不仅是一个代谢酶,更是连接营养感应、能量平衡和细胞命运决定的枢纽。在精准医疗和代谢健康需求日益增长的今天,靶向ACSL5的创新疗法有望成为下一个重磅炸弹级药物,为全球数亿代谢性疾病和肿瘤患者带来新希望。













