- 最新进展
- 产品信息
受体相互作用丝氨酸/苏氨酸激酶2(Receptor-Interacting Serine/Threonine Kinase 2, RIPK2,又称RIP2)是先天免疫信号通路中的关键适配蛋白,作为NOD1/NOD2和Toll样受体(TLRs)的下游信号分子,在炎症性肠病(IBD)、自身免疫性疾病和肿瘤等多种疾病中发挥核心作用。近年来,针对RIPK2的小分子抑制剂研发取得了显著进展,多个候选药物已进入临床试验阶段,展现出良好的治疗前景。
一、RIPK2的生物学功能与信号机制
1.1 分子结构与激活机制
RIPK2是一种含有CARD(Caspase激活与募集结构域)的丝氨酸/苏氨酸激酶,其N端激酶结构域和C端CARD结构域通过中间连接区相连。2025年最新研究通过冷冻电镜技术解析了RIPK2-CARD的寡聚化结构,揭示了“RIPosome”复合物的形成机制:NOD1/NOD2的CARD结构域与RIPK2-CARD相互作用,诱导RIPK2发生寡聚化,从而启动下游信号传导。
1.2 信号通路整合
RIPK2处于多条先天免疫信号通路的交汇点:
- NOD1/NOD2-RIPK2轴:识别细菌肽聚糖成分,激活NF-κB和MAPK通路,诱导促炎细胞因子(TNF-α、IL-6、IL-12/23p40)产生
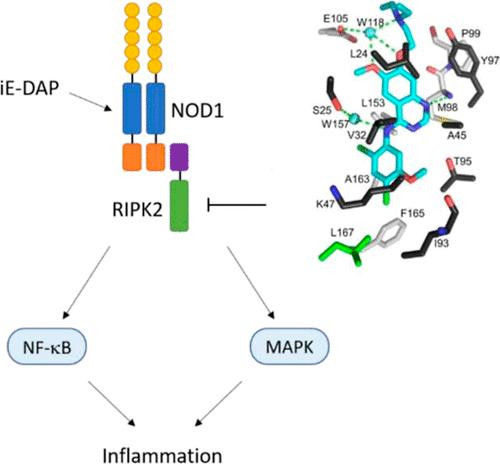
- TLRs-RIPK2轴:Toll样受体通过RIPK2传递信号,在IBD中发挥促炎作用
- 泛素化调控:XIAP、cIAP1/2等E3泛素连接酶介导RIPK2的K63位泛素化,是信号激活的关键步骤
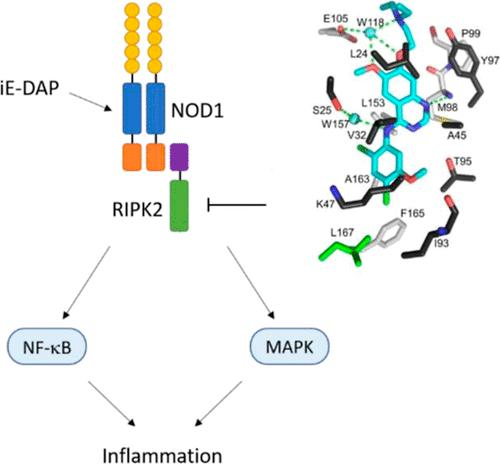
值得注意的是,最新研究表明RIPK2的激酶活性对于NOD2信号传导并非必需,而抑制剂主要通过阻断RIPK2与XIAP的相互作用、抑制RIPK2泛素化来发挥抗炎作用。
二、RIPK2与疾病关联
2.1 炎症性肠病(IBD)
RIPK2在IBD发病机制中扮演双重角色:
- 保护作用:NOD2-RIPK2通路通过激活IRF4和ATG16L1,抑制TLRs诱导的促炎反应,维持肠道免疫稳态
- 致病作用:TLRs-RIPK2通路驱动过度的炎症反应
临床研究显示,克罗恩病(CD)和溃疡性结肠炎(UC)患者结肠黏膜中RIPK2及其信号分子(cIAP2、TRAF6、TAK1)表达显著升高,且与炎症因子水平正相关。NOD2功能缺失突变与CD发病风险增加相关,但有趣的是,IBD患者炎症黏膜中NOD2表达并未升高,提示TLRs-RIPK2通路可能是更有效的治疗靶点。
2.2 肿瘤
2025年4月发表在《Cell Death & Disease》的最新研究揭示了RIPK2在结直肠癌转移中的新机制:RIPK2通过保护YAP蛋白免受ITCH介导的泛素化降解,促进肿瘤转移。这一发现拓展了RIPK2抑制剂在肿瘤治疗中的应用前景。
2.3 其他自身免疫疾病
RIPK2还参与类风湿性关节炎、多发性硬化症、银屑病等疾病的发病过程,使其成为广谱抗炎治疗的潜在靶点。
2.4 代谢性疾病
2026年Endocrine Connections发表的一项研究利用棕榈酸诱导的大鼠L6肌管胰岛素抵抗模型,结果显示,在胰岛素抵抗状态下,RIPK2表达显著升高,而X连锁凋亡抑制蛋白(XIAP)表达降低。
该研究揭示的XIAP-RIPK2调控轴为2型糖尿病的干预提供了新靶点,上述发现提示RIPK2可能也适用于代谢性疾病。通过恢复RIPK2的泛素化修饰或抑制其激酶活性,或可改善胰岛素敏感性和葡萄糖稳态。这一概念的提出拓展了RIPK2靶点的应用场景,从炎症性疾病延伸至代谢紊乱领域。
三、RIPK2抑制剂研发进展
3.1 第一代抑制剂:多靶点激酶抑制剂
早期RIPK2抑制剂多为已上市药物的重新定位:
| 化合物 | 原适应症 | 作用机制 | 特点 |
|---|---|---|---|
| Gefitinib | 非小细胞肺癌 | EGFR抑制剂,Type I | IC₅₀=51 nM,改善SAMP1/YitFc小鼠回肠炎 |
| Erlotinib | 非小细胞肺癌 | EGFR抑制剂,Type I | 与Gefitinib类似机制 |
| Ponatinib | 慢性髓性白血病 | BCR-ABL抑制剂,Type II | FDA批准,强效抑制RIPK2自磷酸化和泛素化 |
| Regorafenib | 结直肠癌 | 多激酶抑制剂,Type II | 临床可用,选择性阻断NOD依赖的炎症信号 |
关键发现:Canning等人(2015)首次证明Type II激酶抑制剂(结合DFG-out构象)对RIPK2的抑制效果比Type I抑制剂提升两个数量级,并解析了RIPK2-Ponatinib共晶结构,发现变构位点可用于选择性抑制剂设计。
3.2 第二代抑制剂:高选择性RIPK2抑制剂
3.2.1 GSK系列(葛兰素史克)
- GSK583:高选择性RIPK2抑制剂,能有效抑制CD患者结肠活检样本中自发性促炎细胞因子释放
- GSK2983559:GSK583的前药,在TNBS诱导的结肠炎模型中显示出与泼尼松龙相当疗效,曾进入I期临床试验(NCT03358407),但因毒理学发现和安全性边际不足而终止开发
3.2.2 大环类抑制剂
OD36和OD38(Tigno-Aranjuez等,2014):
- IC50分别为5.3 nM和14.1 nM
- 高选择性(366激酶谱中仅抑制少数激酶)
- 在SAMP1/YitFc CD模型中下调MDP诱导的炎症因子
- 提出9基因RIPK2激活标志物(GPR84、ICAM1、IRG1等)用于预测患者响应
3.3 临床阶段候选药物
BI 706039(勃林格殷格翰)
- 通过高通量筛选优化获得,结构未公开
- 285激酶谱中仅抑制18个激酶(3 μM浓度)
- 正在开展与Ustekinumab联合治疗CD的临床试验(NCT04978493)
四、新兴治疗策略
4.1 PROTAC降解剂
除传统抑制剂外,基于PROTAC(蛋白降解靶向嵌合体)技术的RIPK2降解剂在IBD临床前模型中展现出卓越疗效,为克服激酶抑制剂耐药性问题提供了新思路。
4.2 靶向蛋白-蛋白相互作用
目前所有RIPK2抑制剂均靶向激酶结构域的ATP结合位点。鉴于RIPK2的CARD-CARD相互作用是信号启动的关键步骤,开发阻断NODs与RIPK2相互作用的变构调节剂代表了一个尚未探索但极具吸引力的方向,有望实现更高的选择性和更少的脱靶效应。
4.3 组织特异性递送
由于RIPK2在多种组织中广泛表达,系统性抑制可能导致副作用。针对IBD等肠道疾病的局部递送策略(如直肠给药的siRNA载体)已在动物模型中验证有效,未来可结合纳米技术实现炎症部位的精准靶向。
结论
RIPK2作为先天免疫信号网络的核心节点,在IBD、自身免疫病和肿瘤等多种疾病中展现出显著的治疗潜力。随着结构生物学研究的深入(如RIPosome复合物解析)和药物化学的进步,从早期多靶点抑制剂到高选择性Type II抑制剂,再到新兴的PROTAC降解剂和变构调节剂,RIPK2靶向治疗正快速走向成熟。BI 706039等候选药物进入临床试验标志着该领域进入转化医学的关键阶段。未来通过解决组织选择性、机制精细调控等挑战,RIPK2抑制剂有望成为炎症性疾病治疗的重要武器。













