- 最新进展
- 产品信息
一、引言
干扰素-γ(IFN-γ)作为Ⅱ型干扰素的唯一成员,在肿瘤免疫调控中呈现复杂的双重功能。一方面,IFN-γ通过激活多种免疫细胞亚群发挥抗肿瘤效应;另一方面,其在特定条件下亦可促进肿瘤进展。这种功能的两面性取决于肿瘤微环境(TME)中的浓度、作用靶细胞类型及其活化状态。全面解析IFN-γ在不同细胞类型中的信号传导与功能结局,对于优化免疫治疗策略具有重要意义。在相关机制研究中,小鼠IFN-γ试剂盒(HICA) 被广泛用于检测不同实验条件下IFN-γ的表达水平,为解析其剂量依赖性与细胞特异性效应提供定量工具。
二、IFN-γ对淋巴细胞亚群的调控
(一)细胞毒性T细胞
细胞毒性T细胞(CTL)既是IFN-γ的主要来源,也是其作用的重要靶细胞。IFN-γ通过Fas-FasL及BIM介导的凋亡途径参与CTL反应的收缩阶段,维持免疫稳态。在CTL扩增阶段,高水平的IFN-γ通过AKT-FOXO1通路下调IL-7Rα表达,限制记忆性T细胞池的形成。诱导IFN-γ产生的免疫治疗虽可促进效应及记忆CD8+T细胞扩增,但其是否通过调控IFNGR及IL-7Rα表达影响细胞长期存活,仍有待阐明。
在小鼠肿瘤模型中,CTL的IFNGR表达水平高于初始T细胞。免疫检查点抑制剂治疗诱导的IFN-γ可导致激活诱导的免疫细胞死亡,限制效应记忆细胞形成,这一机制可能与部分患者的肿瘤逃逸相关。因此,治疗前评估肿瘤负荷、CTL浸润程度及IFN-γ水平,有助于预测治疗反应。
(二)CD4+效应T细胞
与CTL相似,产生IFN-γ的Th1细胞在分化后下调IFNGR2表达,从而提高其在TME中的存活率,发挥抗肿瘤效应。Th1细胞通过T-bet抑制RUNX1,阻止向Th17细胞极化。IFN-γ通过SOCS1及T-bet双重机制抑制Th2极化,分别阻断IL-4受体信号及GATA3功能。TCR刺激下,IFNGR1与STAT1共定位于免疫突触,形成"Th1细胞准备"状态,这一过程可被Th2细胞的IL-4R表达所抑制。值得注意的是,肿瘤浸润效应T细胞上PD-1的表达可抑制Th1分化,形成负反馈回路限制IFN-γ产生。此外,IFN-γ亦可通过降低BCL-2表达、上调Fas/FasL及诱导氧化应激,促进效应CD4+T细胞凋亡。
(三)调节性T细胞
在TME中,IFN-γ可驱动调节性T细胞(Treg)向"脆弱型"表型转化,此类细胞虽维持FOXP3表达但失去抑制活性,从而削弱其促肿瘤功能。Nrp1低表达的Treg亚群与黑色素瘤及头颈部鳞癌患者良好预后相关。
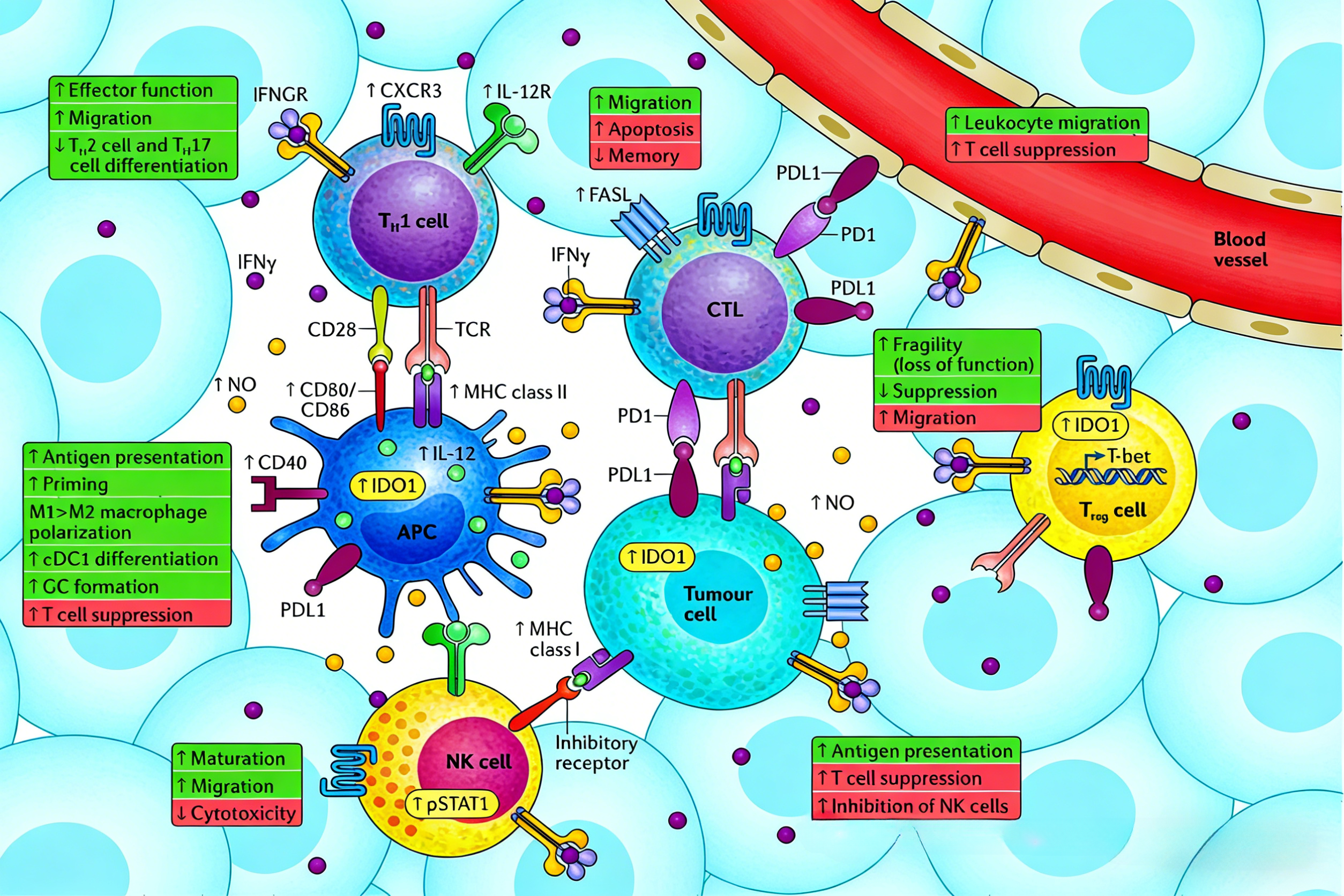
三、IFN-γ对固有免疫细胞的调控
(一)NK细胞
IFN-γ可激活NK细胞的抗肿瘤功能。其肿瘤浸润依赖于IFN-γ诱导的CXCR3表达,IFNGR1或CXCR3基因敲除小鼠均表现为肿瘤浸润NK细胞减少。旁观者T细胞产生的IFN-γ通过TRAIL作用于NK细胞,经IRF1调控增强TRAIL表达,促进NK细胞成熟及肿瘤杀伤功能。
(二)抗原呈递细胞
IFN-γ的关键抗肿瘤功能之一为诱导抗原呈递细胞(APC)表达MHCⅠ类及Ⅱ类分子,促进肿瘤抗原呈递。其通过STAT1、IRF1与CIITAⅣ结合调控MHCⅡ转录,通过IRF1与NLRC5启动子结合调控MHCⅠ表达。同时,IFN-γ诱导共刺激分子CD80及CD86表达,促进T细胞活化。
在树突状细胞(DC)中,IFN-γ驱动其分化为cDC1亚群,表达CD80、CD86、MHCⅠ类、CD40、CD54及CCR7,分泌IL-1β及IL-12,促进Th1分化及CD8+T细胞激活。在B细胞中,IFN-γ与B细胞受体及CD40信号协同,诱导生发中心转录因子BCL-6表达,并与IL-12协同促进抗体类别转换至IgG2a,增强抗体依赖性细胞毒性。
在巨噬细胞中,IFN-γ作为经典的"巨噬细胞激活因子",驱动其向促炎性M1表型极化。其通过下调miR-3473b抑制M2极化,并诱导CXCL9及CXCL10产生,促进免疫细胞浸润并抑制血管生成。
(三)髓系细胞的抑制作用
值得注意的是,IFN-γ亦可诱导DC及肿瘤相关巨噬细胞(TAM)上调IDO及PD-L1等抑制分子,通过代谢调控及促进血管生成推动肿瘤进展。IDO可进一步促进TGF-β产生,驱动Treg分化增殖。IFN-γ还诱导髓系细胞表达iNOS,分解l-精氨酸产生一氧化氮(NO)。NO一方面通过诱导凋亡发挥抗肿瘤作用,另一方面亦可通过p53途径诱导基因组不稳定性及促进血管生成,呈现促肿瘤效应,其具体作用与局部浓度密切相关。
四、IFN-γ对肿瘤细胞的直接调控
肿瘤细胞是TME中对IFN-γ的关键响应者。其抗肿瘤效应主要体现为诱导MHCⅠ类表达及趋化因子CXCL9、CXCL10、CXCL11分泌,促进淋巴细胞迁移并抑制血管生成。然而,CXCL11因与CXCR7结合而具有促血管生成活性;CXCL9及CXCL10促进Th1/Th17效应功能,而CXCL11则通过IL-10诱导Th2及Treg反应。
与APC相似,肿瘤细胞通过MHCⅠ类分子呈递抗原,但MHCⅠ亦可作为"自我"标记抑制NK细胞杀伤。免疫抑制性肿瘤常下调MHCⅠ表达以逃避免疫监视。IFN-γ通过诱导PD-L1、IDO1、iNOS、Fas及FasL表达介导促肿瘤效应。肿瘤细胞是TME中IDO1及NO的重要来源,其iNOS表达促进血管生成,FasL表达诱导免疫效应细胞凋亡。小鼠IFN-γ试剂盒(HICA) 在上述机制研究中用于定量检测IFN-γ水平,为解析其剂量依赖性效应提供了关键数据支撑。
五、提供小鼠IFN-γ 试剂盒 (HICA)的厂商有哪些?
南京优爱生物科技有限公司(UA-Bio)自主研发的 "Mouse IFN-γ Kit (HICA)",是专为研究小鼠Th1型免疫应答与巨噬细胞活化关键通路而打造的高性能体外检测平台。本试剂盒旨在精准、高效地定量检测小鼠干扰素-γ(IFN-γ)蛋白的免疫结合活性,为您在肿瘤免疫、感染免疫、自身免疫病及临床前药物疗效评价等领域的机制研究与临床前药效分析,提供稳定、可靠的标准化解决方案。
| 产品核心优势 |
|---|
| 高纯度与完整生物活性: 试剂盒核心组分采用经多维度质控验证的高纯度、高生物学活性小鼠源IFN-γ蛋白。该蛋白保持正确的天然同源二聚体构象与完整的受体结合能力,能够真实模拟生理状态下小鼠IFN-γ介导的免疫激活信号,确保结合实验数据的准确性、可重复性与功能相关性。 |
| 卓越的批间一致性与稳定性: 依托国际领先的重组蛋白表达平台与高度标准化的纯化工艺,结合严格的放行质控体系,确保产品具备卓越的长期稳定性与极佳的批间一致性。为您长期、连续的临床前研究与高通量筛选工作提供坚实可靠的质量保障。 |
| 即用型灵活检测平台: 本试剂盒基于优化的酶联免疫吸附(ELISA)检测原理,提供预包被板条、高特异性检测抗体、标准品及全套优化的缓冲液体系。操作简便快捷、灵敏度高、特异性强,可广泛适用于抗小鼠IFN-γ抗体/受体拮抗剂筛选、中和活性测定、竞争结合实验、亲和力分析及免疫原性评价等多种研究应用需求。 |
| 完整解决方案与专业支持: 我们提供经充分验证的标准实验方案、典型剂量反应曲线及详尽的结果解读指南,助力您快速建立稳定、可重复的检测流程。南京优爱专业技术团队可为您的研究设计、实验优化及数据分析提供全程、专业的技术咨询与支持。 |
南京优爱生物科技有限公司始终专注于为免疫学、细胞治疗与创新药物研发领域提供前沿、高品质的核心试剂与工具。如需获取关于 "Mouse IFN-γ Kit (HICA)"(货号:UA086046)的详细技术参数、验证数据或具体应用咨询,欢迎随时与我们联系。













