- 最新进展
一、引言
KRAS基因是人类恶性肿瘤中突变频率最高的致癌基因之一,约30%的高死亡率肿瘤与KRAS突变相关。由于其蛋白表面光滑、缺乏典型药物结合口袋,KRAS长期被视为“不可成药”靶点。近年来,靶向KRAS G12C突变亚型的共价抑制剂(如索托拉西布、阿达格拉西布)取得重大突破,相继获批上市,为KRAS突变驱动的恶性肿瘤患者带来希望。然而,临床数据显示,KRAS G12C抑制剂在不同组织来源肿瘤中疗效不一,部分患者存在原发性耐药,另有一部分患者在治疗后迅速出现获得性耐药。目前临床上尚缺乏明确的敏感性生物标志物来预测患者对KRAS G12C抑制剂的治疗反应,难以实现精准治疗。因此,深入揭示KRAS G12C抑制剂的耐药机制并探索克服策略,具有重要的基础研究价值和临床转化意义。人KRAS G12C & VCB Binding 试剂盒(GDP load)作为研究KRAS G12C蛋白与VHL-E3连接酶复合物相互作用的标准化工具,在理解突变蛋白稳定性调控及开发新型降解策略中具有重要应用价值。
二、KRAS G12C抑制剂的临床挑战
KRAS G12C共价抑制剂通过特异性结合突变蛋白GDP结合状态下的变构口袋,将其锁定于非活性构象,从而阻断下游信号传导。尽管该类药物的问世标志着KRAS靶点从“不可成药”走向临床转化,但临床应用中逐渐暴露出耐药性问题。部分KRAS G12C突变肿瘤患者对抑制剂治疗无应答,表现为原发性耐药;另有一些患者在初始治疗后出现疾病进展,提示获得性耐药的发生。不同组织来源的肿瘤对KRAS G12C抑制剂的敏感性也存在显著差异,提示肿瘤微环境和组织特异性因素可能影响药物疗效。这些临床挑战凸显了深入理解耐药机制、寻找预测性生物标志物以及开发联合治疗策略的紧迫性。
三、KRAS G12C耐药机制的新发现
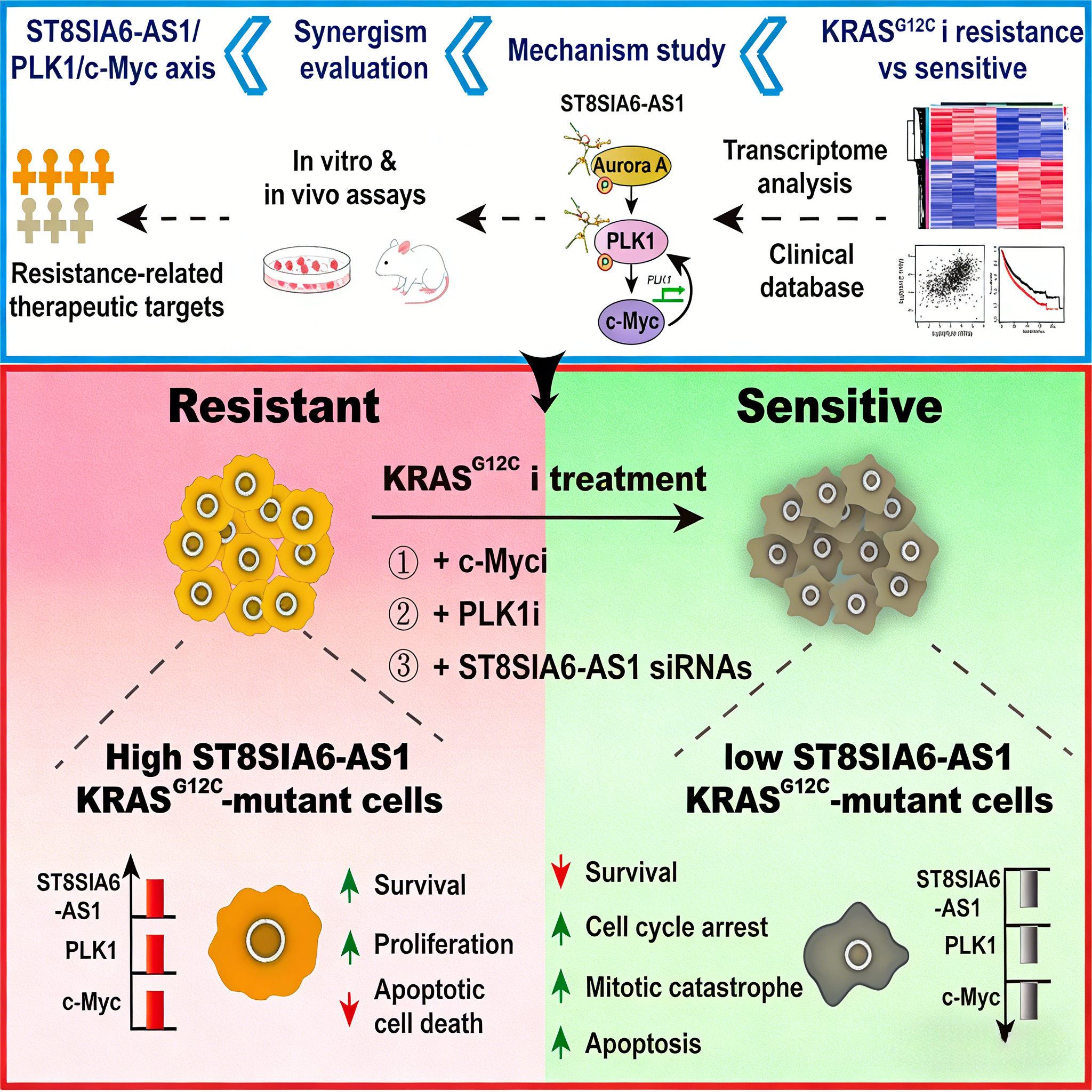
近期研究通过构建KRAS G12C抑制剂获得性耐药细胞株,结合全基因组测序和转录组分析,系统揭示了耐药相关的关键基因和信号通路。研究发现,耐药细胞株中MYC靶基因异常激活,调控细胞G2/M期的关键蛋白Polo样激酶1(PLK1)显著上调。进一步机制研究表明,长链非编码RNA ST8SIA6-AS1在耐药细胞中高表达,可直接与丝/苏氨酸激酶Aurora A和PLK1结合,促进Aurora A介导的PLK1磷酸化激活。活化的PLK1增强c-Myc蛋白S62位点的磷酸化,提高其稳定性;上调的c-Myc作为转录因子,又可直接结合PLK1基因启动子,诱导PLK1转录,形成一个正反馈调控环路。
这一ST8SIA6-AS1/PLK1/c-Myc信号轴的持续活化,在KRAS下游ERK信号被抑制剂阻断的情况下,为肿瘤细胞提供了替代的增殖驱动信号,从而介导对KRAS G12C抑制剂的耐药。研究证实,ST8SIA6-AS1、PLK1和c-Myc的高表达或高活化是驱动细胞对KRAS G12C抑制剂产生耐药性的关键因素之一。
四、克服耐药的新策略
基于上述机制发现,研究人员提出了联合靶向的治疗策略。在裸小鼠移植瘤模型中,KRAS G12C抑制剂与PLK1抑制剂联合应用,可强效抑制KRAS G12C突变肿瘤的生长,并有效克服已建立的耐药。同样,通过siRNA沉默ST8SIA6-AS1表达,也可显著增强耐药细胞对KRAS G12C抑制剂的敏感性。这些结果表明,同时阻断KRAS本身与ST8SIA6-AS1/PLK1/c-Myc信号轴,可实现协同致死效应,为KRAS G12C抑制剂耐药患者提供了新的治疗选择。
该研究还提示,ST8SIA6-AS1和c-Myc的表达丰度可能作为临床评估KRAS G12C抑制剂敏感性和疗效的潜在生物标志物。通过检测这些分子的表达水平,有望在治疗前筛选出可能获益的患者,或在治疗过程中早期识别耐药的发生。
五、人KRAS G12C & VCB Binding 试剂盒的技术原理与应用
在KRAS G12C靶向治疗及耐药机制研究中,准确评估KRAS蛋白的稳定性及其与E3泛素连接酶的相互作用具有重要意义。人KRAS G12C & VCB Binding 试剂盒(GDP load)基于时间分辨荧光共振能量转移(TR-FRET)技术设计,专门用于检测KRAS G12C蛋白与VHL-ElonginC-ElonginB(VCB)复合物之间的相互作用。
VCB复合物是应用最为广泛的E3泛素连接酶之一,在蛋白降解靶向嵌合体(PROTAC)技术中发挥核心作用。该试剂盒利用KRAS G12C蛋白在GDP结合状态下的特定构象,模拟PROTAC分子同时结合靶蛋白和E3连接酶时的三元复合物形成过程。试剂盒提供重组表达的KRAS G12C蛋白和VCB复合物蛋白,分别标记供体荧光基团(如铕穴状化合物)和受体荧光基团(如XL665)。当待测PROTAC分子或阳性对照分子同时结合二者时,供体与受体相互靠近,发生能量转移,产生可定量检测的荧光信号。信号强度与三元复合物的形成效率成正比,从而定量反映KRAS G12C与VCB的接近程度和结合活性。
在耐药机制研究中,该试剂盒可用于评估耐药后出现的KRAS二次突变是否影响其与E3连接酶的相互作用,或用于筛选能够克服耐药的新型PROTAC降解分子。
六、总结与展望
本研究首次揭示了ST8SIA6-AS1/PLK1/c-Myc信号轴在KRAS G12C抑制剂耐药中的核心作用,为理解耐药机制提供了新的视角。联合靶向KRAS与这一信号轴的策略在临床前模型中展现出显著疗效,为克服耐药提供了可行方案。人KRAS G12C & VCB Binding 试剂盒(GDP load)作为研究KRAS G12C与E3连接酶相互作用的关键工具,在耐药机制解析和新型降解剂研发中具有重要应用价值。未来,随着对耐药机制更深入的理解及PROTAC技术的快速发展,针对KRAS G12C的靶向治疗有望实现更持久的疗效和更广泛的适用人群。













