从CAR-T到ADC:Siglec-2/CD22如何改写B细胞恶性肿瘤治疗格局?
本文章讲述了Siglec-2/CD22的作用机理,阐述了Siglec-2/CD22在B细胞发育、活化及功能调控中的表达作用,说明了它们的重要性。
- 最新进展
- 产品信息
- 参考文献
论Siglec-2/CD22如何作用B细胞恶性肿瘤
Siglec-2/CD22是唾液酸结合免疫球蛋白样凝集素(Siglec)家族的重要成员,属于免疫球蛋白基因超家族。作为一种I型跨膜蛋白,Siglec-2/CD22在B细胞发育、活化及功能调控中扮演核心角色,其异常表达与多种恶性疾病和自身免疫性疾病密切相关,已成为当前生物医学研究的热点靶点。
一、Siglec-2/CD22的分子特征与功能机制
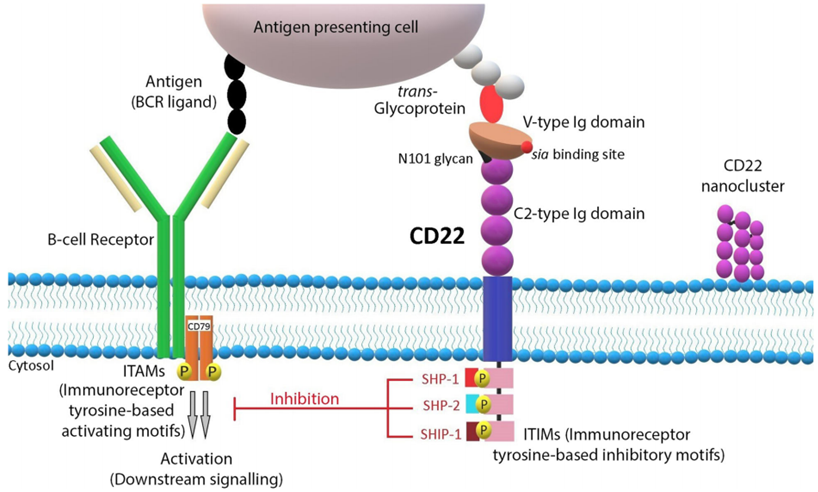
图 Siglec-2/CD22结构和信号通路
Siglec-2/CD22分子量为135 kDa,其胞外段由七个免疫球蛋白样结构域构成,可特异性结合α2,6-连接的唾液酸(α2,6Sia)配体。这种结合通过两种方式调节B细胞功能:
- 顺式相互作用:Siglec-2/CD22与B细胞表面自身唾液酸化配体结合,形成纳米级簇状结构,将其隔离于富含网格蛋白的膜微域中,从而抑制B细胞受体(BCR)信号传导。
- 反式相互作用:Siglec-2/CD22与其他细胞表面唾液酸化配体结合,调节B细胞迁移及BCR信号阈值。当Siglec-2/CD22与BCR交联时,其胞内段免疫受体酪氨酸抑制基序(ITIM)被磷酸化,招募酪氨酸磷酸酶SHP-1,导致下游信号蛋白去磷酸化,最终抑制B细胞活化。
这种双重调控机制使Siglec-2/CD22成为维持体液免疫稳态的关键分子。Siglec-2/CD22缺陷小鼠表现为B细胞过度活化、自身抗体产生增加及系统性自身免疫症状,证实了其在防止自身免疫疾病中的核心作用。
二、Siglec-2/CD22在疾病中的表达异常与致病机制
B细胞恶性肿瘤
Siglec-2/CD22在超过90%的急性淋巴细胞白血病(B-ALL)、非霍奇金淋巴瘤(NHL)及毛细胞白血病(HCL)细胞表面高表达,而在浆细胞中丢失。其表达模式与疾病进展密切相关:
- 耐药机制:CD19 CAR-T治疗后的复发患者中,约30%出现CD19缺失,而Siglec-2/CD22 CAR-T可克服这一耐药性。但部分患者会通过Siglec-2/CD22表达下调(Siglec-2/CD22−/dim疾病)逃逸治疗。
- 预后标志物:Siglec-2/CD22胞吞内化特性使其成为抗体偶联药物(ADC)的理想靶点。高表达Siglec-2/CD22的肿瘤细胞可高效内化ADC,释放细胞毒性药物(如奥加米星),精准杀伤肿瘤细胞。
自身免疫性疾病
Siglec-2/CD22功能缺陷与系统性红斑狼疮(SLE)、类风湿关节炎(RA)等自身免疫病发病相关:
- 信号通路失调:Siglec-2/CD22通过抑制BCR信号,防止自身反应性B细胞活化。Siglec-2/CD22缺陷导致B细胞对自身抗原过度反应,产生抗核抗体等自身抗体。
- 小胶质细胞调控:在阿尔茨海默病(AD)中,Siglec-2/CD22在小胶质细胞表面表达,其与唾液酸化配体结合会抑制小胶质细胞对β-淀粉样蛋白(Aβ)的吞噬作用。血浆可溶性Siglec-2/CD22(sSiglec-2/CD22)水平升高与AD患者脑内Aβ沉积及认知功能下降正相关,提示Siglec-2/CD22可能作为AD生物标志物及治疗靶点。
三、Siglec-2/CD22靶向药物的开发与应用
抗体偶联药物(ADC)
ADC通过抗体特异性结合Siglec-2/CD22,将细胞毒性药物递送至肿瘤细胞:
- 奥英妥珠单抗(Inotuzumab ozogamicin):全球首个获批用于复发/难治性B-ALL的Siglec-2/CD22 ADC,其完全缓解率(CR)达58%,中位总生存期(OS)为7.7个月。
- 莫塞妥莫单抗(Moxetumomab pasudotox):针对毛细胞白血病的Siglec-2/CD22 ADC,通过催化伪毒素抑制蛋白质合成,CR率达41%,且耐受性良好。
CAR-T细胞疗法
Siglec-2/CD22 CAR-T通过基因修饰使T细胞表达靶向Siglec-2/CD22的嵌合抗原受体,已展现显著疗效:
- 临床数据:一项I期试验中,58例Siglec-2/CD22+ B细胞恶性肿瘤患者接受Siglec-2/CD22 CAR-T治疗,CR率达70%,中位OS为13.4个月。但高剂量组(3×10⁶/kg)出现2例5级不良事件(与细胞因子释放综合征相关),提示需优化剂量方案。
- 联合策略:Siglec-2/CD22 CAR-T与CD19 CAR-T联用可克服抗原逃逸,在复发/难治性B-ALL中实现93%的CR率。
单克隆抗体
舒西利单抗(Suciraslimab):全球首个申报上市的Siglec-2/CD22单抗,用于治疗类风湿关节炎。其通过阻断Siglec-2/CD22与唾液酸化配体结合,恢复B细胞信号调控,减少自身抗体产生。
- Epratuzumab:一种免疫调节性Siglec-2/CD22单抗,可诱导Siglec-2/CD22磷酸化并下调BCR表达,在SLE患者中显著降低疾病活动度评分(SLEDAI)。
- Siglec-2/CD22的研究不仅深化了我们对B细胞免疫调控的理解,更为恶性疾病和自身免疫病的治疗提供了创新解决方案。随着靶向技术的不断进步,Siglec-2/CD22有望成为更多疾病领域的关键治疗靶点。
Siglec-2/CD22的研究不仅深化了我们对B细胞免疫调控的理解,更为恶性疾病和自身免疫病的治疗提供了创新解决方案。随着靶向技术的不断进步,Siglec-2/CD22有望成为更多疾病领域的关键治疗靶点。
相关产品推荐
|
货号 |
产品名称 |
表达系统 |
|
Alexa Fluor 647-Labeled Siglec-2/CD22 His Tag Protein, Human |
HEK293 |
|
|
PE-Labeled Siglec-2/CD22 Fc&Avi Tag Protein, Human |
HEK293 |
|
|
PE-Labeled Siglec-2/CD22 His&Avi Tag Protein, Human |
HEK293 |
|
|
Biotinylated Siglec-2 Fc&Avi Tag Protein, Human |
HEK293 |
|
|
Biotinylated Siglec-2 His&Avi Tag Protein, Human |
HEK293 |
|
|
Siglec-2/CD22 His Tag Protein, Human |
HEK293 |
|
|
Siglec-2/CD22 Fc Chimera Protein, Human |
HEK293 |
|
|
Siglec-2/CD22 His Tag Protein, Mouse |
HEK293 |
|
|
Siglec-2/CD22 His Tag Protein, Rat |
HEK293 |
部分数据展示:
Alexa Fluor 647-Labeled Siglec-2/CD22 His Tag Protein, Human 货号: UA011196
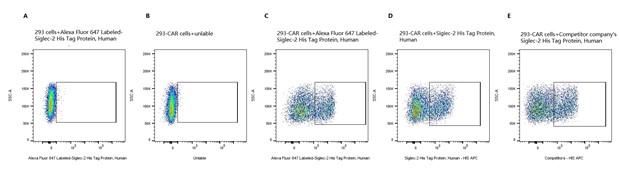
5e5 of transient transfected anti-Siglec-2 ScFv CAR-293 cells were stained with 0.1ug Alexa Fluor 647 Labeled-Siglec-2 His Tag Protein, Human, (Cat. No. UA011196) and unlable respectively (Fig. C and B), and non-transfected 293 cells were used as a control (Fig. A). Alexa Fluor 647 signal was used to evaluate the binding activity.
5e5 of transient transfected anti-Siglec-2 ScFv CAR-293 cells were stained with 0.1ug Siglec-2 His Tag Protein, Human (Cat. No. UA010679) and competitor respectively (Fig. D and E). APC signal was used to evaluate the binding activity.
Biotinylated Siglec-2 Fc&Avi Tag Protein, Human 货号:UA010426
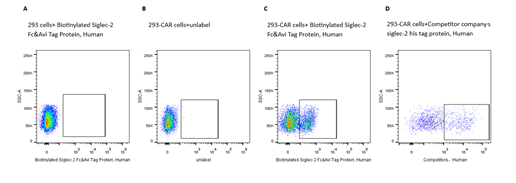
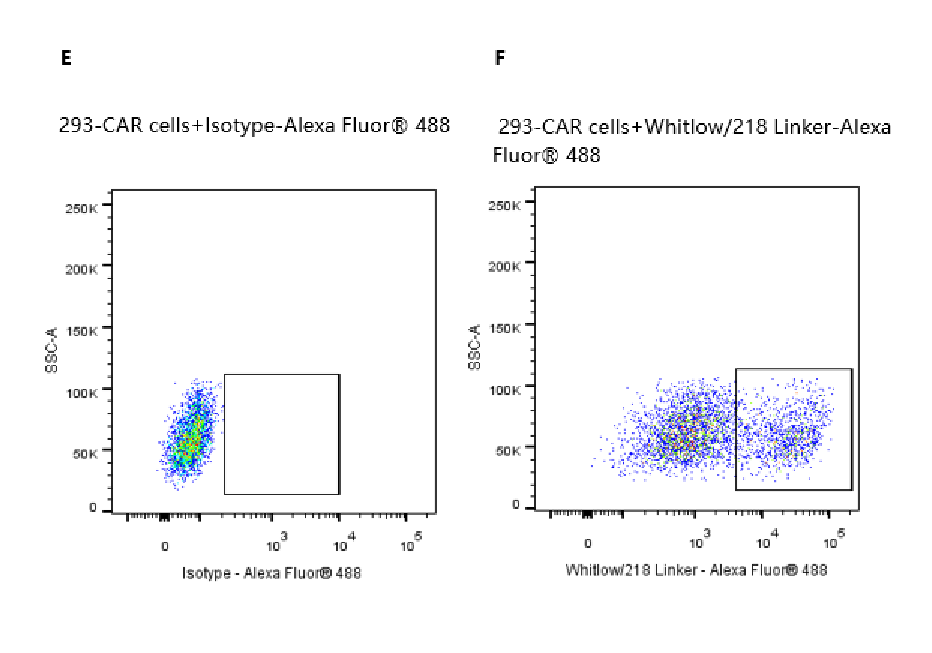
2e5 of transient transfected anti-Siglec-2 ScFv CAR-293 cells were stained with 0.1ug Biotinylated Siglec-2 Fc&Avi Tag Protein, Human, (Cat. No. UA010426) and unlabel respectively (Fig. C and B), and non-transfected 293 cells were used as a control (Fig. A). PE signal was used to evaluate the binding activity. 2e5 of transient transfected anti-Siglec-2 ScFv CAR-293 cells were stained with competitor respectively (Fig. D). APC signal was used to evaluate the binding activity. 2e5 of transient transfected anti-Siglec-2 ScFv CAR-293 cells were stained with isotype and Whitlow/218 Linker-Alexa Fluor® 488 (Fig. E and F). Alexa Fluor® 488 signal was used to evaluate the binding activity.
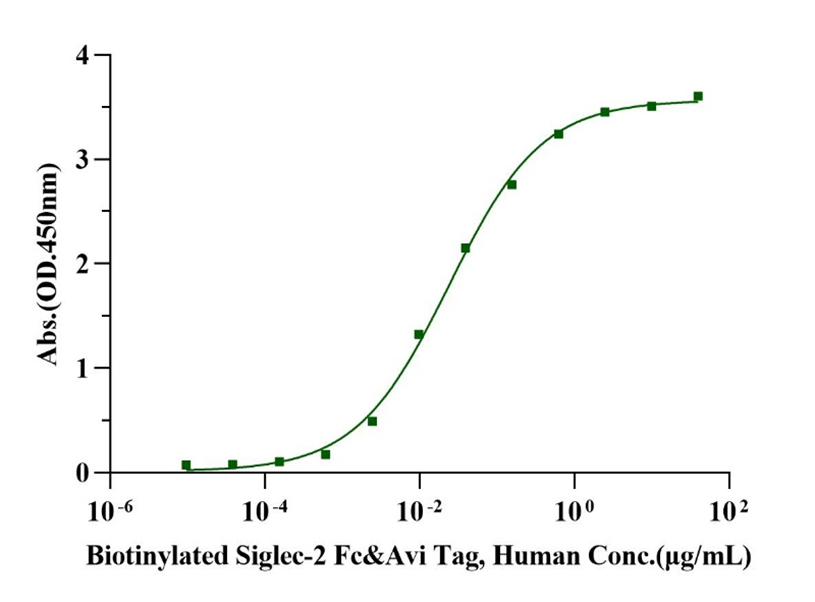
Immobilized Anti-Human CD22 Monoclonal Antibody(Pinbio) at 1.0μg/mL (100μL/well) can bind Biotinylated Siglec-2 Fc&Avi Tag Protein, Human (Cat. No. UA010426) with EC50 of 1.92-2.95ng/mL.
点击下方的产品货号,直达官网详情页供您了解
- Amandeep Aujla; Ravijot Aujla; Delong Liu. Inotuzumab ozogamicin in clinical development for acute lymphoblastic leukemia and non-Hodgkin lymphoma.Biomarker Research.2019.
- Evangelia Kokalaki; Bin Ma; Mathieu Ferrari; Thomas Grothier; Warren Hazelton; et al. Dual targeting of CD19 and CD22 against B-ALL using a novel high-sensitivity aCD22 CAR. Molecular Therapy.2023.
- Lijun Zhao; Shuhong Li; Xiaoyi Wei; Xuexiu Qi; Qiaoru Guo; et al.A novel loop-structure-based bispecifc CAR that targets CD19 and CD22 with enhanced therapeutic effcacy against B-cell malignancies. Protein & Cell.2024.
- Carolin S. Escherich; Zhenhua Li; Kelly R. Barnett; Yizhen Li; Megan Walker; et al. Differentiation-dependent EBF1 Activity Determines CD22 Transcription and Leukemia Sensitivity to Inotuzumab Ozogamicin. Blood.2025.













